
分析 ①取上述溶液少量加入过量Ba(NO3)2溶液,产生白色沉淀,过滤,向沉淀中加入过量的硝酸,沉淀完全溶解,并产生气体,则白色沉淀为碳酸钡,一定不含SO42-;
②向实验①的滤液中滴入AgNO3溶液,出现淡黄色沉淀,沉淀为AgBr,一定含Br-;
③取原溶液与氢氧化钠溶液共热,生成能使湿润红色石蕊试纸变蓝的气体,气体为氨气,一定含NH4+;
④取原溶液进行焰色反应,直接观察,火焰呈黄色,则一定含Na+,再结合离子的反应及离子共存判断.
解答 解:①取上述溶液少量加入过量Ba(NO3)2溶液,产生白色沉淀,过滤,向沉淀中加入过量的硝酸,沉淀完全溶解,并产生气体,则白色沉淀为碳酸钡,一定不含SO42-,则一定含CO32-、可能含HCO3-;由CO32-、Ba2+结合生成沉淀,可知原溶液一定不含Ba2+,由CO32-、H+结合生成水和气体,一定不含H+;
②向实验①的滤液中滴入AgNO3溶液,出现淡黄色沉淀,沉淀为AgBr,一定含Br-;
③取原溶液与氢氧化钠溶液共热,生成能使湿润红色石蕊试纸变蓝的气体,气体为氨气,一定含NH4+;
④取原溶液进行焰色反应,直接观察,火焰呈黄色,则一定含Na+,不能确定是否含K+,
综上所述,该溶液中肯定存在的离子有NH4+、Na+、CO32-、Br-;肯定不存在的离子为Ba2+、H+、SO42-;不能确定是否存在的离子为K+、HCO3-,
故答案为:NH4+、Na+、CO32-、Br-;Ba2+、H+、SO42-;K+、HCO3-.
点评 本题考查无机物的推断及离子反应,为高频考点,把握实验流程中的反应、现象及离子推断为解答的关键,侧重分析与推断能力的考查,注意离子反应及元素化合物知识的综合应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 用瓷坩埚熔融氢氧化钠或碳酸钠 | |
| B. | 用玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH值 | |
| C. | 取用金属钠、钾时,未用完的钠、钾应放回原瓶 | |
| D. | 读取量筒内液体的体积,俯视读数会导致读数偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入氧气的一极为正极,发生氧化反应 | |
| B. | 该电池负极的电极反应为2H2-4e-=4H+ | |
| C. | 该电池工作一段时间,电解质溶液浓度保持不变 | |
| D. | 该电池在工作时,溶液中的阴离子向负极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操 作 | 现 象 |
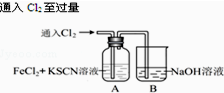 | I.A中溶液变红 Ⅱ.稍后,溶液由红色变为黄色 |
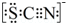 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+、Na+、SO42-、Cu2+ | B. | Ba2+、Mg2+、Cl-、SO42- | ||
| C. | H+、K+、OH-、NO3- | D. | NO3-、I-、H+、Mg2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-一定存在,且c(Cl-)≥0.4 mol/L | |
| B. | SO42-、NH4+一定存在,Cl-可能不存在 | |
| C. | CO32-、Al3+一定不存在,K+可能存在 | |
| D. | 至少存在5种离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
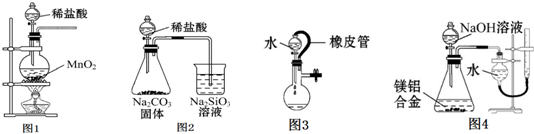
| A. | 用图1所示装置制取少量Cl2 | |
| B. | 用图2所示装置证明非金属性Cl>C>Si | |
| C. | 图3所示装置中水不能持续流下,说明装置气密性良好 | |
| D. | 用图4所示装置测定镁铝合金中铝的质量分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和氯气在光照条件下反应:2CH4+Cl2$\stackrel{光照}{→}$2CH3 Cl+H2 | |
| B. | 实验室用电石制乙炔:CaC2+2H2O→Ca(OH)2+HC≡CH↑ | |
| C. | 用NaOH溶液中和苯酚溶液的酸性:H++OH-═H2O | |
| D. | 向苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2 C6H5OH+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
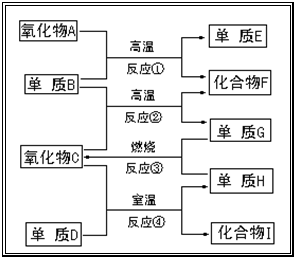
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com