
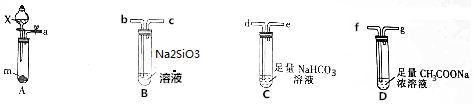
分析 较强酸能和弱酸盐反应生成弱酸,元素的非金属性越强,其最高价氧化物的水化物酸性越强,要验证物质酸性强弱顺序为H2SO3>CH3COOH>H2CO3>H2SiO3,应该用A制取二氧化硫、用D装置生成乙酸、用C装置生成二氧化碳、用D装置生成硅酸即可,再结合题目分析解答.
解答 解:较强酸能和弱酸盐反应生成弱酸,元素的非金属性越强,其最高价氧化物的水化物酸性越强,要验证物质酸性强弱顺序为H2SO3>CH3COOH>H2CO3>H2SiO3,应该用A制取二氧化硫、用D装置生成乙酸、用C装置生成二氧化碳、用D装置生成硅酸即可,
(1)仪器X的名称是分液漏斗,用浓硫酸制取二氧化硫,其盛装的液体试剂是浓硫酸,故答案为:浓硫酸;
(2)该整套装置中应该用A制取二氧化硫、用D装置生成乙酸、用C装置生成二氧化碳、用D装置生成硅酸,所以装置D需微热,按气流从左到右的顺序连接好仪器a→f,g→d,e→b,
故答案为:f;g;d;b;
(3)试剂m是一种正盐,焰色反应为黄色,说明含有Na元素,浓硫酸和亚硫酸钠反应生成二氧化硫,反应方程式为H2SO4(浓)+Na2SO3=Na2SO4+H2O+SO2↑,则M的化学式是Na2SO3,
故答案为:Na2SO3;
(4)装置B中为二氧化碳和硅酸钠溶液的反应,发生反应的离子方程式为CO2+H2O+SiO32-=CO32-+H2SiO3↓,
故答案为:CO2+H2O+SiO32-=CO32-+H2SiO3↓,
(5)装置D中足量的CH3COONa浓溶液的作用除可以产生CH3COOH蒸气外,还能验证酸性H2SO3>CH3COOH,故答案为:验证酸性H2SO3>CH3COOH.
点评 本题考查性质实验方案设计题,为高频考点,侧重考查学生实验设计及实验操作能力,明确实验原理及实验目的是解本题关键,熟练掌握元素化合物性质及转化,注意A制取二氧化硫时不能用稀盐酸,因为盐酸挥发出的HCl能和乙酸钠反应生成乙酸而干扰实验,为易错点.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C2H4 | B. | C2H2和C2H4 | C. | C2H4和C2H6 | D. | C4H8和C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1LpH=2的HCl溶液中,由水电离出的H+的数目0.01NA | |
| B. | 标准状况下,2.24L的CCl4中含有的氯原子数为0.4NA | |
| C. | 常温下,1molCO2中含有的共用电子对数目为2NA | |
| D. | 标准状况下,2.24L Cl2与水充分反应,转移的电子数小于0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeC13和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 | |
| B. | 其他条件不变,向稀H2SO4与过量Zn的混合物中加少量铜片,既能增大H2生成速率,又能减小生成H2的物质的量 | |
| C. | 其他条件不变,加热或加压都能使H2(g)+I2(g)?2HI(g)的v正和v逆同时增大 | |
| D. | v=$\frac{△c}{△t}$是化学上表示化学反应速率的唯一方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡时体系能量的变化 | ||
| A | B | C | ||
| ① | 2 | 1 | 0 | 0.75Q kJ |
| ② | 0.4 | 0.2 | 1.6 | |
| A. | 容器①、②中反应的平衡常数均为18 | |
| B. | 容器②中达到平衡时放出的热量为0.05Q kJ | |
| C. | 向容器①中通入氦气,平衡时A的转化率增大 | |
| D. | 其他条件不变,若容器②保持恒容绝热,则达到平衡时C的体积分数小于2/3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
| SiF4 | -90 | -86 | 易水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com