
下列溶液中的氯离子浓度与50 mL 1 mol·L-1的AlCl3溶液中氯离子浓度相等的是
A.75 mL 2 mol·L-1的CaCl2 B.75 mL 1 mol·L-1的NH4Cl
C.150 mL 1 mol·L-1的NaCl D.150 mL 3 mol·L-1的KCl
科目:高中化学 来源:2017届山东省滕州市高三上学期10月月考化学试卷(解析版) 题型:选择题
金属镍有广泛的用途粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A.阳极发生还原反应,其电极反应式:Ni2+ + 2e— Ni
Ni
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.电解后,溶液中存在的金属阳离子只有Fe2+ 和Zn2+
D.电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上9月月考化学试卷(解析版) 题型:填空题
【化学―选修3:物质结构与性质】硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布图为___________。
(2)锗、砷、硒的第一电离能大小排序为_____________。(用元素符号表示)
(3)SeO32-的中心原子杂化类型是___________;SeO32-的立体构型是_____________;与SeO32-互为等电体的分子有(写一种物质的化学式即可)_____________。
(4)H2Se属于___________(填:极性或非极性)分子;比较H2O、H2Se的沸点高低:H2O_________H2Se(填“>”“<”或“=”),其原因是_____________。单质硒的熔点为217℃ ,它属于____________晶体。
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为_________;若该晶胞密度为pg·cm-3,硒化锌的摩尔质量为Mg/mol。NA代表阿伏加德罗常数,则晶胞参数a为_______pm。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上期初化学卷(解析版) 题型:选择题
将30 mL 0.5 mol·L-1的NaCl溶液加水稀释到500 mL,稀释后溶液中NaCl的物质的量浓度为
A.0.03 mol·L-1 B.0.3 mol·L-1
C.0.05 mol·L-1 D.0.04  mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上期初化学卷(解析版) 题型:选择题
用NA表示阿伏德罗常数,下列叙述正确的是
A.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
B.标准状况下,22.4LH2O含有的分子数为 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量为0.5 mol的MgCl2中,含有Mg2+个数为 NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上期初化学卷(解析版) 题型:选择题
下列说法不正确的是
A.浊液的分散质粒子直径大于l00nm,不能通过滤纸
B.胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸
C.利用丁达尔效应可以区分溶液和胶体
D.将氯化铁浓溶液和氢氧化钠浓溶液混合,能得到氢氧化铁胶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上第一次月考化学卷(解析版) 题型:填空题
在容积为2.0L的密闭容器内,物质D在T℃时发生反应。其反应物和生成物的物质的量随时间t的变化关系如下图,据图回答下列问题:
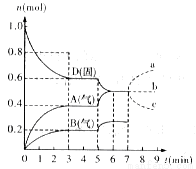
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为___________mol/(L•min)。(结果保留两位有效数字)
(2)根据右图写出该反应的化学方程式___________。
(3)第5分钟时,升高温度,A、B、D的物质的量变化如图,则该反应是___________(填“放热”或“吸热”)反应,若在第7分钟时增加D的物质的量,A的物质的量变化正确的是___________(用图中a~c的编号回答)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高一上第一次考试化学卷(解析版) 题型:推断题
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:
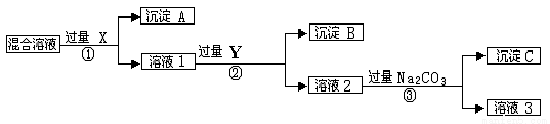
请回答下列问题:
(1)写出实验流程中下列物质的化学式。试剂X : ,沉淀A: ,试剂Y: ,沉淀B: 。
(2)上述实验流程中加入过量的Na2CO3的目的是 。
(3)按此实验方案得到的溶液3中肯定含有 (填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的 ,之后若要获得固体NaNO3需进行的实验操作是 (填操作名称)。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上第12次周测化学卷(解析版) 题型:选择题
一定温度下,下列溶液中的粒子浓度关系式正确的是
A.0.1mol·L-1的NaHS溶液中:c(OH-)=c(H+)+c(H2S)
B.往氯化铵溶液中加水 的值变大
的值变大
C.0.1mol·L-1的NaOH溶液与0.2mol·L的HA溶液等体积混合,所得溶液呈碱性:c(Na+)>c(HA)>c(A-)>c(OH-)>c(H+)
D.pH相等的①NH4Cl ②NH4Al(SO4)2 ③NH4HSO4溶液中,c(NH4+)大小顺序:①>②>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com