
| A、①② | B、②③ | C、①④ | D、③④ |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属腐蚀的实质就是金属原子失去电子被还原的过程 |
| B、为了使原电池能持续稳定的产生电流需使用盐桥,盐桥中的阳离子应向负极迁移 |
| C、牺牲阳极的阴极保护法和外加电源的阴极保护法利用的都是电解原理 |
| D、铅蓄电池充电时溶液的pH值逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
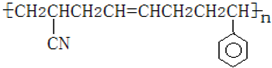
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、反应的化学方程式为:2M?N |
| B、0~t1时间段内,平均反应速率v(N)﹕v(M)=2﹕1 |
| C、t2时,正逆反应速率相等,达到平衡 |
| D、t3时,正反应速率大于逆反应速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 .有甲、乙、丙、丁四个同学将其命名依次为:2,2-二甲基-4-乙基戊烷;3,5,5-三甲基己烷;4,4-二甲基-2-乙基戊烷;2,2,4-三甲基己烷.下列对四位同学的命名判断中正确的是( )
.有甲、乙、丙、丁四个同学将其命名依次为:2,2-二甲基-4-乙基戊烷;3,5,5-三甲基己烷;4,4-二甲基-2-乙基戊烷;2,2,4-三甲基己烷.下列对四位同学的命名判断中正确的是( )| A、甲的命名主链选择是正确的 |
| B、乙的命名编号是错误的 |
| C、丙的命名主链选择是正确的 |
| D、丁的命名是错误的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com