
分析 A,B,C,D四种化合物,分别由K+、Ba2+、SO42-、CO32-、OH-中的两种离子组成(离子可重复使用),
①A不溶于水和盐酸,则A只能为BaSO4;
②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E,E为CO2,可知B为BaCO3;
③C的水溶液呈碱性,与硫酸反应生成A,则C为Ba(OH)2;
④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊,D为可溶性碳酸盐,只能为K2CO3,以此来解答.
解答 解:由K+、Ba2+、SO42-、CO32-、OH-中的两种离子组成的化合物中,硫酸钡不溶于水和酸,碳酸钡不溶于水、可溶于盐酸,氢氧化钡为强碱,碳酸钾为可溶性盐,
由①A不溶于水和盐酸,则A只能为BaSO4;
②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E,E为CO2,可知B为BaCO3;
③C的水溶液呈碱性,与硫酸反应生成A,则C为Ba(OH)2;
④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊,D为可溶性碳酸盐,只能为K2CO3,
故答案为:BaSO4;BaCO3;Ba(OH)2;K2CO3.
点评 本题考查无机物的推断,为高频考点,把握离子结合成的物质、物质的性质和发生的反应为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:解答题
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1 mol CO、 2 mol H2 | 1 mol CH3OH | 2 mol CH3OH | |
| 平衡 时数 据 | 反应能量变化的绝对值(kJ) | a | b | c |
| 反应物转化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
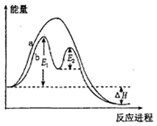
| A. | 反应过程a有催化剂参与 | |
| B. | 该反应为吸热反应 | |
| C. | 改变催化剂,可改变该反应的活化能 | |
| D. | 有催化剂条件下,反应的活化能等于E1+E2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
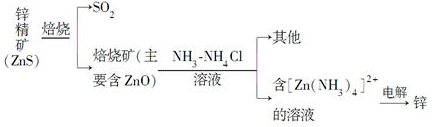
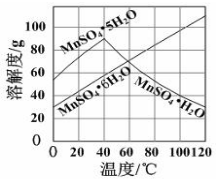
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
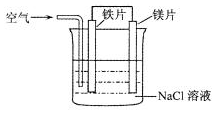
| A. | 镁片为负极,镁片上产生黄绿色气体 | |
| B. | 铁片为阳极,铁片上产生无色气体 | |
| C. | 溶液中铁片与镁片之间产生白色沉淀 | |
| D. | 溶液的pH将逐渐增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ(H2)=0.1 mol•L-1•min-1 | B. | υ(N2)=0.2 mol•L-1•min-1 | ||
| C. | υ(NH3)=0.15 mol•L-1•min-1 | D. | υ(H2)=0.3 mol•L-1•min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com