
【题目】下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:1的是( )
A.![]()
B.
C.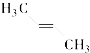
D.
【答案】C
【解析】解:化合物的核磁共振氢谱中出现2种峰,说明有机物中含有2种类型的氢原子,且原子数之比为3:1;
A、 ![]() 中含有三种等效氢原子,应出现三种峰值,故A错误;
中含有三种等效氢原子,应出现三种峰值,故A错误;
B、 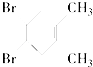 中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为6:4=3:2,故B错误;
中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为6:4=3:2,故B错误;
C、  中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为3:1,故C正确;
中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为3:1,故C正确;
D、 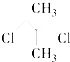 中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为6:4=3:2,故D错误;
中含有两种等效氢,出现两种峰值,且不同峰值的氢原子个数比为6:4=3:2,故D错误;
故选:C.
根据核磁共振氢谱中峰的种数等于氢原子的种类,峰面积之比等于个数之比,然后根据等效氢判断.
等效氢原子:①分子中同一甲基上连接的氢原子等效,②同一碳原子所连甲基上的氢原子等效,③处于镜面对称位置上的氢原子等效.


科目:高中化学 来源: 题型:
【题目】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料,制取氧化钴的流程如下。
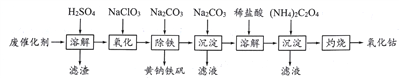
(1)溶解:溶解后过滤,将滤渣洗涤2~3次,洗液与滤液合并,其目的是__________________。
(2)氧化:加热搅拌条件下加入NaC1O3,其作用是_______________________________。
(3)除铁:加入适量的Na2CO3调节酸度,生成黄钠铁矾Na2[Fe6(SO4)4(OH)12]沉淀。写出该反应的化学方程式:__________________________________________________。
(4)沉淀:生成沉淀碱式碳酸钴[(CoCO3)2·3Co(OH)2],沉淀需洗涤,检验沉淀是否洗涤干净的操作是_________________________________________________________。
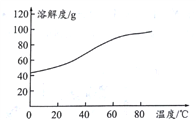
(5)溶解:CoCl2的溶解度曲线如图所示。向碱式碳酸钴中加入足量稀盐酸,边加热边搅拌至完全溶解后,需趁热过滤,其原因是__________________________________。
(6)灼烧:准确称取所得CoC2O4固体2.205g,在空气中灼烧得到钴的一种氧化物1.205g,写出该氧化物的化学式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水常用Cl2杀菌消毒,使水中含有Cl-,为了检验Cl-的存在,可选用的试剂是( )
A.酚酞溶液B.FeCl3溶液C.AgNO3溶液D.NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨浸菱锌矿制备活性氧化锌,成本低,选择性好,其工艺流程如下:
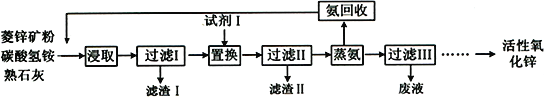
(1)滤渣Ⅰ主要成分的化学式为__________。
(2)浸取液中含少量Pb2+、Cu2+等重金属离子,可加入试剂Ⅰ除去,试剂Ⅰ为______________,但在实际操作过程中实际加入量远高于理论量,可能的原因是____________________________。
(3)过滤Ⅱ后得到Zn(NH3)4CO3溶液,经直接蒸汽加热可析出碱式碳酸锌[ZnCO3·2Zn(OH)2·H2O]沉淀,其反应化学方程式为____________________________。
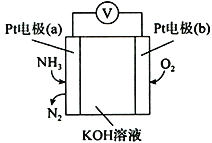
(4)蒸氨过程中会有部分氨气逸出,可用电化学气敏传感器监测环境中NH3的含量,原理如图所示。负极的电极反应为________________________________,假设蒸氨过程中逸出氨气16.8L (标准状况)进入传感器,另一极需要通入标准状况下O2的体积为____________________。
(5)蒸氨完成时,废液中残余氨含量需小于0.2mol/L,如果残余氨浓度过低,蒸汽用量增大,回收氨水中氨浓度降低,不利于循环使用;如果残余氨浓度过高,会导致____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠俗名纯碱或苏打,在外观上与食盐相似,可用于洗涤,如清洗厨房用具的油污等。请你至少用两种方法区分厨房中用的食盐与纯碱__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应:KIO3+6HI===3I2+KI+3H2O中,氧化产物与还原产物的物质的量之比为( )
A. 1∶1 B. 6∶1
C. 1∶5 D. 5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果Fe3+、SO42-、Al3+和M四种离子以物质的量之比2∶4∶1∶1共存于同一溶液中,那么M可能是( )
A. Na+ B. OH- C. Cl- D. CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com