
| A. | 1:1 | B. | 3:4 | C. | 9:8 | D. | 4:3 |
分析 把Fe3O4和铝粉配成铝热剂,分成两等份,一份在高温下恰好完全反应生成铁与氧化铝,由电子转移守恒可知$\frac{8}{3}$n(Fe)=3n(Al),然后将生成物与足量的稀盐酸反应,铁与盐酸反应生成氯化亚铁与氢气,由电子转移守恒可知n(H2)=n(Fe);令一份直接加入足量的NaOH溶液使之充分反应,铝与氢氧化钠反应生成偏铝酸钠与氢气,由电子转移守恒可知2n′(H2)=3n(Al),据此计算判断.
解答 解:把Fe3O4和铝粉配成铝热剂,分成两等份,一份在高温下恰好完全反应生成铁与氧化铝,由电子转移守恒可知$\frac{8}{3}$n(Fe)=3n(Al),然后将生成物与足量的稀盐酸反应,铁与盐酸反应生成氯化亚铁与氢气,由电子转移守恒可知n(H2)=n(Fe),所以n(H2)=$\frac{9}{8}$n(Al);
令一份直接加入足量的NaOH溶液使之充分反应,铝与氢氧化钠反应生成偏铝酸钠与氢气,由电子转移守恒可知2n′(H2)=3n(Al),所以n′(H2)=$\frac{3}{2}$n(Al).
故两种情况下生成气体的物质的量之比为n(H2):n′(H2)=$\frac{9}{8}$n(Al):$\frac{3}{2}$n(Al)=3:4,故选:B.
点评 本题考查混合物的计算、根据方程式的计算,难度中等,本题采取电子转移守恒计算,比根据方程式简单容易,清楚反应过程是关键,注意混合物的计算中守恒的运用.


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:推断题
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | Li | Be | B | C | N | O | F |
| 3 | Na | Mg | Al | Si | P | S | Cl |
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳和水反应吸收131.3kJ 能量 | |
| B. | 1mol 碳和1mol 水反应生成一氧化碳和氢气并吸收131.3kJ 热量 | |
| C. | 1mol 固态碳和1mol 水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ | |
| D. | 1 个固态碳原子和1 分子水蒸气反应吸热131.1kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:
将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:99 | B. | 1:100 | C. | 100:1 | D. | 99:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{△}^{氧化/催化剂}$
$→_{△}^{氧化/催化剂}$ $→_{△}^{H_{2}/Ni}$
$→_{△}^{H_{2}/Ni}$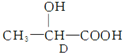
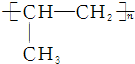 .
.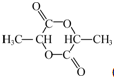 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com