
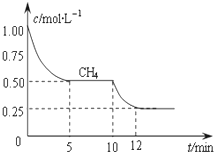
 �ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϣ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
�ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϣ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
| 1.00mol/L-0.50mol/L |
| 5min |
| 2.0��2.0 |
| 0.5��8.5 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��31g�������������ף����������ʵĺ�����Ʒ�У�������NA����ԭ�� |
| B������1mol�Ȼ�����ȫת��Ϊ�����������壬���ɢϵ�н�������С��NA |
| C��1molNa2O2��ˮ��Ӧת�Ƶĵ�����ΪNA |
| D��58.5g���Ȼ��ƹ����к���NA���Ȼ��Ʒ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||
B��
| ||
C��
| ||
D��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��262.6 kJ?mol-1 |
| B��-131.3 kJ?mol-1 |
| C��-352.3 kJ?mol-1 |
| D��131.3 kJ?mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������������ܶȱ��ֲ��� |
| B��v����N2��=3 v����H2�� |
| C���������ƽ����Է����������� |
| D��������Ũ���ǵ���Ũ�ȵ�2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��NH4Cl |
| B��NaOH |
| C��Na2CO3 |
| D��Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ȡ5mL 0.1mol/L KI��Һ���μ�0.1mol/L FeCl3��Һ5��6�Σ���������2mL CCl4�������ȡ�ϲ���Һ���μ�KSCN��Һ����Һ����Ѫ��ɫ��֤����Һ�л�����Fe3+ |
| B�������������ⸯʴʵ���У��ڸ�����Χ����K3[Fe��CN��6]��Һ�������ɫ���� |
| C��ȼ�ϵ��ʵ���У���KNO3��Һ��Na2SO4��Һ��������ˮ��Ч��Ҫ�õö� |
| D�����ǵġ��������ʵ����ֻ������Ũ�������ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
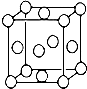 ij��λ������Ϊ����ɫ���壬��ԭ���������������A��B��C��D��E����Ԫ����ɣ���ԭ�Ӹ�����Ϊl4��4��5��1��1�� ����C��DԪ��ͬ������ԭ������DΪC�Ķ�����EԪ�ص���Χ�����Ų�Ϊ��n-1��dn+6nsl���ش��������⣮
ij��λ������Ϊ����ɫ���壬��ԭ���������������A��B��C��D��E����Ԫ����ɣ���ԭ�Ӹ�����Ϊl4��4��5��1��1�� ����C��DԪ��ͬ������ԭ������DΪC�Ķ�����EԪ�ص���Χ�����Ų�Ϊ��n-1��dn+6nsl���ش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��ѧʽ | Zn��OH��2 | ZnS | AgCl | Ag2S | MgCO3 | Mg��OH��2 |
| �ܶȻ� | 5��10-17 | 2.5��10-22 | 1.8��10-10 | 6.3��10-50 | 6.8��10-6 | 1.8��10-11 |
| A��2AgCl+Na2S�T2NaCl+Ag2S | ||||
B��MgCO3+H2O
| ||||
| C��ZnS+2H2O�TZn��OH��2+H2S�� | ||||
| D��Mg��HCO3��2+2Ca��OH��2�TMg��OH��2��+2CaCO3��+2H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com