
| A. | HNO3、KOH、FeCl3 | B. | K2SO4、KCl、HCl | ||
| C. | AgNO3、HCl、KCl | D. | Na2CO3、KCl、BaCl2 |
分析 A.KOH、FeCl3结合生成红褐色沉淀;
B.该组物质之间不反应,且均为无色;
C.AgNO3分别与HCl、KCl结合生成白色沉淀;
D.Na2CO3、BaCl2结合生成白色沉淀.
解答 解:A.KOH、FeCl3结合生成红褐色沉淀,且FeCl3为黄色,与无色不符,故A不选;
B.该组物质之间不反应,可大量共存,且均为无色,得到无色透明溶液,故B选;
C.AgNO3分别与HCl、KCl结合生成白色沉淀,溶液变浑浊,故C不选;
D.Na2CO3、BaCl2结合生成白色沉淀,溶液变浑浊,故D不选;
故选B.
点评 本题考查离子的共存,为高频考点,把握常见离子之间的反应、离子的颜色为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 研究物质的性质时,常用到观察、实验、分类、比较等方法 | |
| B. | 研究物质性质的一般程序的第一步是预测物质的性质 | |
| C. | 可以用分类的方法预测物质的性质 | |
| D. | 观察是一种有计划、有目的地用感官考察研究对象的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量 | 0.255g | 0.385g | 0.459g |
| 气体体积 | 280mL | 336mL | 336mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9:1:6 | B. | 3:1:2 | C. | 3:2:2 | D. | 9:2:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含金属元素的离子不一定都是阳离子 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 化合物变为单质时,化合价变化的元素一定被还原 | |
| D. | 油锅着火时,立即用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
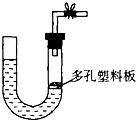 如图是气体制取装置,下列能用此装置制取气体并能“随开随用、随关随停”的是( )
如图是气体制取装置,下列能用此装置制取气体并能“随开随用、随关随停”的是( )| A. | 大理石和稀硫酸制取二氧化碳 | B. | 锌粒和稀硫酸制氢气 | ||
| C. | 块状碳酸钠和稀盐酸制取二氧化碳 | D. | 氯酸钾和二氧化锰制氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
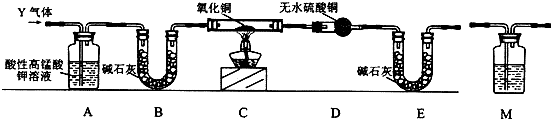
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com