
| A. | pH=10的CH3COONa溶液中,水电离产生的c(OH-)=1×10-10mol•L-1 | |
| B. | pH=a的氨水溶液,稀释10倍(溶液体积变为原来10倍)后,其pH=b,则a=b+1 | |
| C. | pH=3的H2S溶液与pH=11的NaOH溶液任意比例混合:C(Na+)+c(H+)=c(OH-)+c(HS-) | |
| D. | pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的:c(Na+)大小顺序为 ①>②>③ |
分析 A.醋酸钠溶液中醋酸根离子结合水电离出氢离子水解,促进水电离平衡正向进行,溶液显碱性,氢氧根全部是水电离出;
B、一水合氨为弱电解质,存在电离平衡;
C.溶液中存在电荷守恒分析,阴阳离子所带电荷总数相同;
D.对应酸的酸性越弱,其盐的水解程度越大,溶液的碱性越强,溶液PH越大;当PH相同时,酸越强,盐的浓度越大.
解答 解:A.pH=10的CH3COONa溶液中,水电离产生的c(OH-)水=c(H+)水=$\frac{1{0}^{-14}}{1{0}^{-10}}$=1×10-4mol•L-1,故A错误;
B.一水合氨为弱电解质,存在电离平衡,将将pH=a的氨水溶液稀释10倍后,则电离平衡被促进,故pH的变化小于1,故b>a-1,故B错误;
C.pH=3的H2S溶液与pH=11的NaOH溶液任意比例混合溶液中存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),故C错误;
D.在相同的条件下测得①CH3COONa②NaHCO3③NaClO三种溶液pH相同,已知酸性:CH3COOH>HClO>HCO3-,所以水解程度:NaClO>NaHCO3>CH3COONa,pH相同时,溶液的浓度:NaClO<NaHCO3<CH3COONa,即①>②>③,c(Na+)大小顺序为 ①>②>③,故D正确;
故选D.
点评 本题考查了电离平衡的移动以及弱电解质溶液稀释时溶液pH的变化规律,并考查了强酸强碱的酸式盐溶液中水电离出的氢离子浓度的计算,掌握酸和碱对水的电离有抑制作用,而盐类的水解对水的电离有促进作用是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | SiO2不溶于水,因此不属于酸性氧化物 | |
| B. | CO2通入水玻璃中可得硅酸,说明碳酸酸性大于硅酸 | |
| C. | SiO2是酸性氧化物,它不溶于任何酸 | |
| D. | SiO2晶体由SiO2分子构成,1个Si原子连接2个O原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
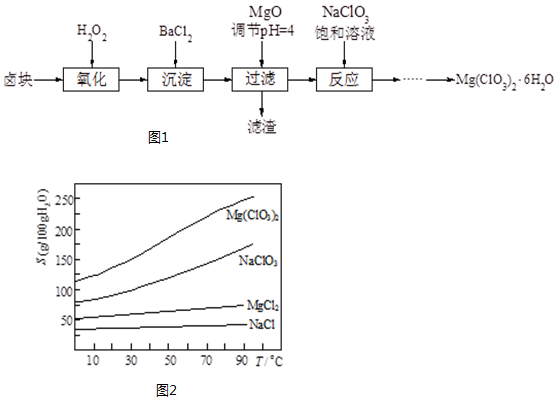
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4、C2H4 | B. | C2H4、C4H8 | C. | C2H6、C2H2 | D. | C2H4、C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①④⑤ | C. | ②③ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com