
| A. | 研制乙醇汽油代替汽油作汽车燃料 | |
| B. | 采用银作催化剂,用乙烯和氧气反应制取环氧乙烷( ) ) | |
| C. | 在萃取操作的演示实验中,将CCl4萃取溴水改为CCl4萃取碘水 | |
| D. | 用铜和稀HNO3反应制取Cu(NO3)2 |
分析 绿色化学又称“环境无害化学”、“环境友好化学”、“清洁化学”,绿色化学的最大特点是在始端就采用预防污染的科学手段,因而过程和终端均为零排放或零污染.化合反应是一变多的反应,把所有原料都转化成了期望中的产品,实现了绿色化学的理念.
解答 解:A.乙醇汽油能代替汽油作为燃料,减少污染,符合绿色化学理念,故A正确;
B.采用银作催化剂乙烯和氧气制取环氧乙烷原子利用率100%,符合绿色化学理念,故B正确;
C.碘水比溴水污染小,溴水有毒,故符合绿色化学理念,故C正确;
D.用铜和稀HNO3反应制取Cu(NO3)2反应过程中有一氧化氮气体有毒生成,不符合绿色化学理念,故D错误.
故选D.
点评 本题考查绿色化学,只要抓住题干中所给出的“绿色化学”的要求,即可顺利作答,较简单.


科目:高中化学 来源: 题型:解答题
 实验题(一)在实验室配制100mL0.5mol/L的Na2CO3溶液,请回答下列问题
实验题(一)在实验室配制100mL0.5mol/L的Na2CO3溶液,请回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
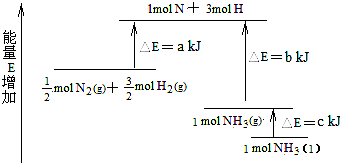
| A. | N2(g)+H2(g)=NH3(l)△H=+(b+c-a)kJ•mol-1 | |
| B. | N2(g)+3H2(g)=2NH3(g)△H=+2(b-a)kJ•mol-1 | |
| C. | N2(g)+3H2(g)=2NH3(l)△H=-2(b+c-a)kJ•mol-1 | |
| D. | N2(g)+H2(g)=NH3(g)△H=+(a+b)kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 熔点:Na>K>Rb | B. | 沸点:NH3<PH3<AsH3 | ||
| C. | 热稳定性:PH3>H2O>HF | D. | 酸性:HClO>H2SO4>H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
| ② | 在FeCl2溶液中加入锌片 | Zn+Fe2+=Zn2++Fe | ||
| ③ | 在FeCl3溶液中加入足量铁粉 | Fe3+具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S | B. | C | C. | Cl | D. | F |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
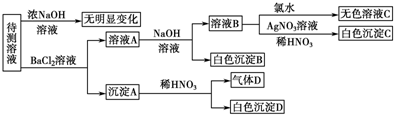
| 肯定存在的离子 | 肯定没有的离子 | |
| 化学式或离子符号 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
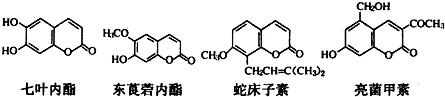
| A. | 七叶内酯与东茛菪内酯互为同系物 | |
| B. | 四种化合物含有的官能团种类完全相同 | |
| C. | l mol上述四种物质与足量氢氧化钠溶液反应,消耗氢氧化钠最多的是亮菌甲素 | |
| D. | 它们都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com