
金属镍、铁及非金属元素碳在合金材料、有机合成材料中有广泛的应用。请回答下列问题:
(1)Ni原子的核外电子排布式为 。
(2)Fe原子的外围电子排布图为 。
(3)含碳化合物丙烯腈(H2C=CH—C≡N)分子中碳原子轨道杂化类型为
(4)NiO、FeO的晶体类型均与氯化钠晶体相同,Ni2+和Fe2+离子半径分别为69 Pm和78 Pm,则两种物质的熔点NiO FeO(填“>”或“<”),判断依据是 。
(5)CaC2晶体的晶胞也与氯化钠相似,但由于CaC2晶体中的C22-存在,使晶胞沿一个方向拉长,则CaC2晶体中1个C22-周围距离最近且相等的Ca2+数目为 ,C22-与O22+互为等电子体,写出O22+的电子式 。
(6)铁在一定条件下可形成体心立方堆积的晶体,设铁原子半径为r,请用含r的代数式表示该晶体空间利用率 。
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是( )

(2)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用下图表达。
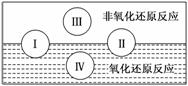
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
________________________________________________________________________,
其中水为________剂。
(3)氯化铵常用作焊接。如在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:____CuO+____NH4Cl ____Cu+____CuCl2+____N2↑+____H2O。
____Cu+____CuCl2+____N2↑+____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是________(填元素名称) ,氧化剂是____________(填化学式)。
,氧化剂是____________(填化学式)。
③反应中若产生0.2 mol的气体,则有________ mol的电子转移。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有机化合物中均含有酸性杂质,除去这些杂质的方法中正确的是( )
A.苯中含苯酚杂质:加入溴水,过滤
B.乙醇中含乙酸杂质:加入碳酸钠溶液洗涤,分液
C.乙醛中含乙酸杂质:加入氢氧化钠溶液洗涤,分液
D.乙酸丁酯中含乙酸杂质:加入碳酸钠溶液洗涤,分液
查看答案和解析>>
科目:高中化学 来源: 题型:
将0.2mol某饱和一元醇完全燃烧后,生成的气体缓慢通过盛有0.5L 2mol/L的氢氧化钠溶液中,生成两种钠盐Na2CO3 与 NaHCO3的物质的量之比为1:3,
(1)求该一元醇的分子式。 (2)该醇有几种结构中含羟基的同分异构体。
(3)写出(2)中能被氧化为醛的结构简式。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应10AgF +5Cl2 + 5H2O =9AgCl + AgClO3 + 10HF + O2。若有1mol氧气生成时反应中转移电子
A.4mol B.9mol C.10mol D.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2和Cl2均可用于漂白工业,对于二者的说法正确的是( )
A.利用SO2的漂白性可使酸性高锰酸钾溶液褪色
B.漂白粉是一种混合物,其有效成分是 Ca(ClO)2
C.为便于储存和使用,可用液氯代替氯水漂白干燥棉布上的有色物质
D.为增强漂白效果,可将等物质的量的SO2和Cl2混合使用以达到增强效果的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

下列描述正确的是( )
A.反应开始到10 s,用Z表示的反应速率为0.158 mol/(L•s)
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol/L
C.反应开始到10 s时,Y的转化率为79.0 %
D.反应的化学方程式为:X(g)+Y(g)=Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体,但不能干燥有较强还原性的HI、H2S等气体
B.浓硫酸与单质硫反应的方程式为:S+2H2SO4(浓) 3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
3SO2↑+2H2O,在此反应中,浓硫酸既表现了其强氧化性又表现了其酸性
C.把足量铜粉投入到只含H2SO4 2 mol的浓硫酸中,得到气体体积标准状况下为22.4 L
D.常温下能够用铁、铝等容器盛放浓H2SO4,是因为浓H2SO4的强氧化性使其钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
碳、氢、氧三种元素组成的有机物A,相对分子质量为102,含氢的质量分数为9.8%,分子中氢原子数为氧原子数的5倍。
(1)A的分子式是________。
(2)A有2个不同的含氧官能团,其名称是________________ ________________________________________________________。
(3)一定条件下,A与氢气反应生成B,B分子的结构可视为1个碳原子上连接2个甲基和另外2个结构相同的基团。则A的结构简式是________。
(4)写出两个与A具有相同官能团,并带有支链的同分异构体的结构简式:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com