
����Ŀ����һ���������ܱ������м���2mol A��0.6molC��һ������B�������塣һ�������·�����Ӧ��������Ũ����ʱ��仯��ͼһ��ʾ��ͼ��Ϊt2ʱ�̺�ı䷴Ӧ������ƽ����ϵ�з�Ӧ������ʱ��仯����������ĸ��ζ����ı�һ�ֲ�ͬ����������֪t3-t4��Ϊʹ�ô�����ͼһ��t0-t1��c(B)δ������

��1����t1=15min����t0-t1����CŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊv(C)=___________��
��2��t4-t5�θı������Ϊ____________��B����ʼ���ʵ���Ϊ____________������ƽ��ʱ��Ӧ��ƽ�ⳣ�����±���ʾ��
t1-t2 | t2-t3 | t3-t4 | t4-t5 | t5-t6 |
K1 | K2 | K3 | K4 | K5 |
K1��K2��K3��K4��K5֮��Ĺ�ϵΪ____________(����>������<������=������)��
��3��t5-t6�α����������¶Ȳ��䣬��A�����ʵ������仯��0.01mol�����˹����������������Ƚ�������ΪakJ��д�����¶��¸÷�Ӧ���Ȼ�ѧ����ʽ____________��
���𰸡���1��0.02mol/(L��min)��
��2����Сѹǿ��1.0mol��K1=K2=K3=K4<K5��
��3��2A(g)+B(g) ![]() 3C(g) ��H=+200akJ/mol��
3C(g) ��H=+200akJ/mol��
��������
�����������1��15min�ڣ���CŨ�ȱ仯��ʾ�ķ�Ӧ����Ϊv(C)=![]() =0.02 mol/(Lmin)���ʴ�Ϊ��0.02 mol/(Lmin)��
=0.02 mol/(Lmin)���ʴ�Ϊ��0.02 mol/(Lmin)��
��2��t3��t4��t4��t5������ƽ���Dz��ƶ��ģ���ֻ����ѹǿ�ʹ���Ӱ��ģ����Ӧ���ƶϸ÷�ӦΪ������仯�ķ�Ӧ��t3��t4��ƽ���ԭƽ�������Ҫ�죬��t4��t5�������ֱ�������ǰ��Ӧ�ǼӴ�������Ϊ����ֻ����һ�Σ�t4��t5��Ϊ��ѹ����Ӧ���Ũ�Ƚ��ͣ��������Ũ�������ͼһ��֪��AΪ��Ӧ�CΪ�����A�ı仯Ϊ0.2mol/L��C�ı仯��Ϊ0.3mol/L�������ڸ÷�ӦΪ������仯�ķ�Ӧ������BΪ��Ӧ����ݻ�ѧ��Ӧ������֮�ȵ��ڻ�ѧ����ʽǰ�ļ���ϵ���ȣ��÷�Ӧ�ķ���ʽΪ2A(g)+B(g) ![]() 3C(g)�����ԣ���c(B)=
3C(g)�����ԣ���c(B)=![]() ��n(A)=
��n(A)=![]() ��0.2mol/L=0.1mol/L����ʼ2molA����Ӧ��Ũ��Ϊ1mol/L�������Ӧ��
��0.2mol/L=0.1mol/L����ʼ2molA����Ӧ��Ũ��Ϊ1mol/L�������Ӧ��![]() =2L����B����ʼ���ʵ���Ϊn(B)=(0.1mol/L+0.4mol/L)��2L=1mol��t1-t2�Σ�����ƽ��״̬��c(A)ƽ��=0.8mol/L��c(B)ƽ��=0.4mol/L��c(C)ƽ��=0.6mol/L��K1=
=2L����B����ʼ���ʵ���Ϊn(B)=(0.1mol/L+0.4mol/L)��2L=1mol��t1-t2�Σ�����ƽ��״̬��c(A)ƽ��=0.8mol/L��c(B)ƽ��=0.4mol/L��c(C)ƽ��=0.6mol/L��K1=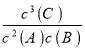 =
=![]() =0.84��t2-t3�Σ�Ϊ�ı�Ũ�ȣ�ƽ���ƶ���ƽ�ⳣ�����䣬K2=0.84��t3-t4�Σ�ʹ�ô������ӿ췴Ӧ��ƽ�ⳣ�����䣬K3=0.84��t4-t5�Σ�Ϊ����ѹǿ����Ӧ���ʽ��ͣ�ƽ�ⲻ�ƶ���ƽ�ⳣ�����䣬K4=0.84��t5-t6�Σ�Ϊ�����¶ȣ�ƽ��������Ӧ�����ƶ���ƽ�ⳣ������ K1=K2=K3=K4��K5���ʴ�Ϊ����Сѹǿ��1.0mol��K1=K2=K3=K4��K5��
=0.84��t2-t3�Σ�Ϊ�ı�Ũ�ȣ�ƽ���ƶ���ƽ�ⳣ�����䣬K2=0.84��t3-t4�Σ�ʹ�ô������ӿ췴Ӧ��ƽ�ⳣ�����䣬K3=0.84��t4-t5�Σ�Ϊ����ѹǿ����Ӧ���ʽ��ͣ�ƽ�ⲻ�ƶ���ƽ�ⳣ�����䣬K4=0.84��t5-t6�Σ�Ϊ�����¶ȣ�ƽ��������Ӧ�����ƶ���ƽ�ⳣ������ K1=K2=K3=K4��K5���ʴ�Ϊ����Сѹǿ��1.0mol��K1=K2=K3=K4��K5��
��3�����ݷ���ʽ���㣬��A�����ʵ������仯��0.01mol�����˹����������������Ƚ�������Ϊa kJ����Ӧ2molAʱ����������200akJ������ͼ���֪��t5��t6��ӦΪ�����¶ȣ�����Ӧ���ʴ����淴Ӧ���ʣ�ƽ��������Ӧ�����ƶ���������ӦΪ���ȷ�Ӧ�������Ȼ�ѧ����ʽΪ2A(g)+B(g) ![]() 3C(g)��H=+200a kJ/mol���ʴ�Ϊ��2A(g)+B(g)
3C(g)��H=+200a kJ/mol���ʴ�Ϊ��2A(g)+B(g) ![]() 3C(g)��H=+200a kJ/mol��
3C(g)��H=+200a kJ/mol��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵��������ȷ���� ( )
A���������ǣ�C12H19Cl3O8��������Ȼ��������ζ��
B��δ�������ƻ��������Ʊ���ɫ������ƻ����֭�ܷ���������Ӧ
C�����������ķ��������������롢�ᴿ������
D����ȩ��֬���ϳ����л������������л��߷��ӻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ͬ��Ba(OH)2��Һ�У��ֱ�������ʵ���Ũ����ȵ�H2SO4��NaHSO4��Һ���䵼�������������Һ����仯��������ͼ��ʾ�����з�����ȷ������ ��
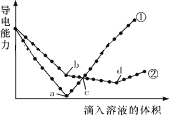
A���������μ�H2SO4��Һ�ı仯����
B��b����Һ�д������ڵ�������SO42-��Na����OH��
C��a��d�����Ӧ����Һ��������
D��c������Һ�к�����ͬ����OH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ�����͵����ǽ������ϣ����㷺Ӧ���ڼ��ɵ�·�����������Ʊ���Ӧԭ��Ϊ��Al2O3+N2+3C�T2AlN+3CO���Ʊ������У�ԭ����Ȳ�����Ӧ����ȫ�����ض�����ɲ�Ʒ�к���̼��Al2O3�����ʣ�Ϊ�ⶨ��Ʒ��AlN������������ijͬѧ����ͼ1װ�ý������ʵ�飮��ѡ�õĻ�ѧ�Լ�Ϊ��mg������Ƭ״���塢NaOH������Һ��ˮ��ú�͡�ҽ�þƾ����ش��������⣺

��1����װ��ʵ��װ�ã�ʹ��ǰ��һ��Ӧ��
��2��ͼ1��B�����Լ����ѡ�� ������ţ���
��ú�� ��ҽ�þƾ� ��ˮ
��֪A ����NaAlO2���ɣ����ų��д̼�����ζ���壬д��A�з�����Ӧ����������ʽ ��
��3����ȡC����Ͳ����Һ�����ʱ��Ӧע���������⣬������� ������ţ�
a��C��Һ�治������ʱ��������
b�������ƶ�C��ʹ֮Һ����B��Һ����ƽ
c��A�в����������ݳ�
d�������밼Һ����ʹ���ƽ
��4��mg������������NaOH������Һ��Ӧ��ʵ�������C���ռ���Һ������ΪVL��������ɱ�״��������AlN��Ʒ�Ĵ���Ϊ ��д�������ʽ����
��5������ʵ�鷽��������������������������������ϴ����˽����������A��B����װ���е�һ�֣���ͨ����ڽ��У���ֻ����м��ֱ�Ҫ�����ݲ�д�����������ͿɱȽ�ȷȷ����Ʒ��AlN��������������������װ���ǣ� ������ţ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���3�������Ϊ1.0L�ĺ����ܱ������У���Ӧ2H2(g)+CO(g) ![]() CH3OH(g)�ﵽƽ�⡣����˵������ȷ����( )
CH3OH(g)�ﵽƽ�⡣����˵������ȷ����( )
���� | �¶�/�� | ���ʵ���ʼŨ��/molL-1 | ���ʵ�ƽ��Ũ��/molL-1 | ||
c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
�� | 400 | 0.20 | 0.10 | 0 | 0.080 |
�� | 400 | 0.40 | 0.20 | 0 | |
�� | 500 | 0 | 0 | 0.10 | 0.025 |
A���÷�Ӧ������Ӧ����
B���ﵽƽ��ʱ���������з�Ӧ��ת���ʱ��������е�С
C���ﵽƽ��ʱ����������c(H2)������������c(H2)������
D���ﵽƽ��ʱ���������еķ�Ӧ���ʱ��������еĴ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʽ2H2��g����O2��g����2H2O��l����H1����571.6kJ��mol��1������ڷ���ʽ2H2O��l����2H2��g����O2��g����H2��?��˵������ȷ������ ��
A������ʽ�л�ѧ��������ʾ������
B���÷�Ӧ����H2����571.6kJ��mol��1
C���÷�Ӧ��H2������
D���÷�Ӧ�ɱ�ʾ18gˮ�ֽ�ʱ����ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڹ�ҵ�ϣ��ϳɰ����Ʊ�����һ��������������������£�

��1���ϳ����з�����ӦN2(g)+3H2(g)![]() 2NH3(g)��H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1___________300��(����>������<������=��)��
2NH3(g)��H<0���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������T1___________300��(����>������<������=��)��
![]()
��2�������ڴ�����ȼ�գ�����һ�ֵ��ʺ�ˮ����ѧ�����ô�ԭ������Ƴɰ���������ȼ�ϵ�أ��������ҺΪKOH�����缫������Ӧ�ĵ缫��ӦʽΪ___________________��
��3����80��ʱ����ͭ��Ũ���ᷴӦ�õ���0.40mol N2O4�������2L�Ѿ���յĹ̶����ܱ������з�����ӦN2O4 (g)![]() 2NO2(g)����H>0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
2NO2(g)����H>0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�

������a=_________�����¶�ʱ�÷�Ӧ��ƽ�ⳣ��K=____________��
���ı�����ʹ��Ӧ���´ﵽƽ�⣬��ʹc(NO2)/c(N2O4)ֵ��С�Ĵ�ʩ��___________(�����)��
A������N2O4����ʼŨ�� B�������¶� C��ʹ�ø�Ч���� D������������ͨ��ϡ������
��4�����᳧��β��ֱ���ŷŽ���Ⱦ������Ŀǰ��ѧ��̽������ȼ�������еļ��齫���������ﻹԭΪ������ˮ����Ӧ����Ϊ��CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g) ��H=��574kJmol��1
4NO(g)+CO2(g)+2H2O(g) ��H=��574kJmol��1
CH4(g)+4NO(g)![]() 2N2(g)+CO2(g)+2H2O(g) ��H=��1160kJmol��1
2N2(g)+CO2(g)+2H2O(g) ��H=��1160kJmol��1
�����ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ��____________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ��H=-1 025kJ/mol���÷�Ӧ��һ�����淴Ӧ������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����( )
4NO(g)+6H2O(g) ��H=-1 025kJ/mol���÷�Ӧ��һ�����淴Ӧ������Ӧ����ʼ���ʵ�����ͬ�����й��ڸ÷�Ӧ��ʾ��ͼ����ȷ����( )

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��t��ʱ����3molA��lmolB����ͨ�����Ϊ2L���ܱ�������(�����ݻ�����)���������·�Ӧ��3 A(g)+B(g) ![]() xC(g) ��H<0����2minʱ�ﵽƽ��״̬(�¶Ȳ���)ʣ����0.8molB�������C��Ũ��Ϊ0.4mol/L������д�пհף�
xC(g) ��H<0����2minʱ�ﵽƽ��״̬(�¶Ȳ���)ʣ����0.8molB�������C��Ũ��Ϊ0.4mol/L������д�пհף�
��1���ӿ�ʼ��Ӧ���ﵽƽ��״̬������B��ƽ����Ӧ����Ϊ__________��
��2��x=___________��ƽ�ֳ���K=___________��
��3����������ԭƽ�������������ͨ���������� (���赪����A��B��C������Ӧ)��ѧƽ��(����ĸ)____ ________����ͨ������A��ѧƽ�⽫___________��
A��������Ӧ�����ƶ� B�����淴Ӧ�����ƶ� C�����ƶ�
��4������ԭƽ��������������ٳ���amolC����t��ʱ�ﵽ�µ�ƽ�⣬��ʱB�����ʵ���Ϊn(B)��__________mol��
��5�����������Ӧ����ͬ�¶Ⱥ������н��У���ʹ��Ӧ�ﵽƽ��ʱC�����ʵ���������ԭƽ����ȣ���ʼ������������ʵ����ʵķ�n (A)��n(B)��n(C)֮��Ӧ������Ĺ�ϵʽΪ___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com