
| A、氯化钠 | B、固体硝酸铵 |
| C、固体氧化钠 | D、固体氢氧化钠 |
科目:高中化学 来源: 题型:
| A、Fe3+、Na+、SO32-、I- |
| B、H+、NO3-、SO42-、Fe2+ |
| C、Cu2+、Mg2+、SO42-、NO3- |
| D、NH4+、Ba2+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A、最简单气态氢化物的热稳定性:R>Q |
| B、最高价氧化物对应水化物的酸性:Q<W |
| C、原子半径:T>Q>R |
| D、R的最高价氧化物对应的水化物和它的氢化物反应不能生成盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
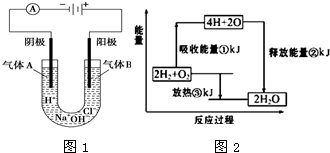 (1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化.已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收 249kJ的能量;形成水分子中1mol H-O键能够释放 463kJ能量.如图1表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上.
(1)在化学反应中,随着物质的变化,化学能也发生改变,还可能伴随着不同形式的能量转化.已知:破坏1mol氢气中的化学键需要吸收436kJ能量;破坏1/2mol氧气中的化学键需要吸收 249kJ的能量;形成水分子中1mol H-O键能够释放 463kJ能量.如图1表示氢气和氧气反应过程中能量的变化,请将图中①、②、③的能量变化的数值,填在相应的横线上.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、随核电荷数的增加,碱金属元素和卤素的熔沸点都逐渐降低 |
| B、碱金属元素中,锂原子失去最外层电子的能力最弱;卤素中,氟原子得电子的能力最强 |
| C、钾与水的反应比钠与水的反应更剧烈 |
| D、溴单质与H2的反应比碘单质与H2的反应更剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH4HCO3和盐酸的反应是放热反应 |
| B、该反应中,热能转化为产物内部的能量 |
| C、反应物的总能量高于生成物的总能量 |
| D、反应的热化学方程式为:NH4HCO3+HCl→NH4Cl+CO2↑+H2O H>0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com