
下列现象中不是由于人类日常生活和生产对生态环境的破坏而产生的是
[ ]
科目:高中化学 来源: 题型:013
1953年日本九州南部熊本县水俣镇发生了水俣事件,致使许多人中毒乃至死亡.水俣病主要是由于水中的汞以甲基汞形式存在,通过食物链进入生物体内,造成中毒现象.下列关于甲基汞的叙述中,错误的是
[ ]
A.甲基汞是一种剧毒物质
B.甲基汞被摄入人体后能迅速排出,不会蓄积
C.甲基汞对人体的破坏主要在于会使脑萎缩,侵害神经细胞,破坏掌握身体平衡的小脑和知觉系统
D.熊本县发生水俣事件的主要原因是工厂污水不加以处理就排放
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
1953年日本九州南部熊本县水俣镇发生了水俣事件,致使许多人中毒乃至死亡.水俣病主要是由于水中的汞以甲基汞形式存在,通过食物链进入生物体内,造成中毒现象.下列关于甲基汞的叙述中,错误的是
[ ]
A.甲基汞是一种剧毒物质
B.甲基汞被摄入人体后能迅速排出,不会蓄积
C.甲基汞对人体的破坏主要在于会使脑萎缩,侵害神经细胞,破坏掌握身体平衡的小脑和知觉系统
D.熊本县发生水俣事件的主要原因是工厂污水不加以处理就排放
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.人体血糖浓度的相对稳定受多种因素影响。现有甲、乙、丙三人.甲正常,乙的胰岛B细胞被自身免疫反应所破坏.丙的胰岛B细胞功能正常、体内含有抗胰岛素受体的抗体。
请回答下列问题:
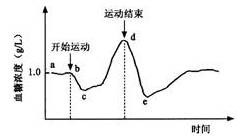
(1).甲在某次运动前后血糖浓度的变化如右图所示。bc段血糖浓度下降的直接原因是
_ __, cd段血糖浓度升高主要是由于血液中肾上腺素和__ _ 的明显增加引起的。
(2).用斐林试剂对甲、乙、丙三人空腹时尿样进行检测,水浴加热后观察到砖红色的是__ _。
(3).给丙注射胰岛素 ___(填“能“或“不能”)有效调节其血糖水平,原因是_ __。
Ⅱ.人体体温能够保持相对恒定,是由于产热量和散热量保持动态平衡的结果。请回答:
(1)当身体的冷觉感受器受到寒冷刺激时,产生的兴奋由 传至下丘脑体温调节中枢,可引起 分泌增多,该激素作用于全身细胞,提高细胞代谢的速度,增加产热量;在38℃的高温环境中,人体主要通过 方式散热。
(2)当体内有炎症时会出现发热现象,这有利于吞噬细胞和抗菌物质等转移炎症区,抵御病原体的攻击,此过程属于 免疫。人体注射乙型流感疫苗后,通过体液免疫和细胞免疫,产生的相应 不能识别并作用于侵入机体的甲型H1N1流感病毒。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省无锡一中高二上学期期中考试化学试卷(必修) 题型:填空题
(1)油脂被摄入人体后,在酶的作用下水解为 和甘油(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)发育出现障碍,患营养缺乏症,这主要是由于摄取_________(填“蛋白质”、“脂肪”或“糖类”)不足引起的。下列食物中富含该物质的是 (填字母)。
| A.菠菜 | B.花生油 | C.瘦肉 | D.西瓜 |
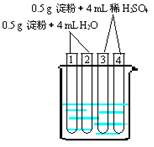
| 编号 | 操作 | 现象 |
| 1 | 加入碘水 | 溶液变成蓝色 |
| 2 | 加入银氨溶液,水浴加热 | 未出现银镜 |
| 3 | 加入碘水 | 溶液变成蓝色 |
| 4 | 加入银氨溶液,水浴加热 | 未出现银镜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
甲同学设计以下实验制取氧气和氧化铜。
(1)制取氧气
①用20%的![]() 溶液,通过反应
溶液,通过反应![]() 来制取氧气,则在下列A、B、C三装置中最佳装置是_____
来制取氧气,则在下列A、B、C三装置中最佳装置是_____

②与气体发生装置相连接的D装置的导管口是_____
③为了能使产生的氧气被充分干燥,可采取的操作是
(2)制取氧化铜
将m g铜粉在氧气流中加热到高温,使铜粉全部氧化,得n g粉末X。乙同学查阅资料知: 铜与氧气的反应有:①![]() ,②
,②![]() ;在酸性条件下:
;在酸性条件下:![]() 。由此得出结论:铜虽然全部氧化,但由于加热温度偏高,产物不一定是纯CuO,可能含有一定量的氧化亚铜(
。由此得出结论:铜虽然全部氧化,但由于加热温度偏高,产物不一定是纯CuO,可能含有一定量的氧化亚铜(![]() )。
)。
(3)探究铜的氧化物的成分
为测定粉末X中是否含有![]() ,甲、乙、丙三同学分别设计如下实验方案。
,甲、乙、丙三同学分别设计如下实验方案。
甲同学的实验方案是:向粉末X中加入稀硫酸,若有___ ,则说明固体中含有![]() 。
。
乙同学的实验方案是:再将粉末X放人氧气中加热,如果其质量增加,则说明其中含有![]() 。
。
丙同学的实验方案是:通过分析实验数据就可以确定粉末X的成分。若n的取值范围是![]() ,则粉末X中含有
,则粉末X中含有![]() ,其物质的量是_____。
,其物质的量是_____。
请你再设计一个与上述三个实验方案中现象均不相同的实验方案,通过对化学反应和对实验现象的分析来确定粉末X中是否含有![]() 。写出该实验中反应的离子方程式。
。写出该实验中反应的离子方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com