
反应C(s)+H2O(g)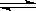 CO(g)+ H2(g)在一容积可变的密闭容器中进行。下列条件的改变对其反应速率几乎无影响的是( )
CO(g)+ H2(g)在一容积可变的密闭容器中进行。下列条件的改变对其反应速率几乎无影响的是( )
A.压缩容器体积,增大体系压强
B.加入适当的催化剂
C.保持压强不变,充入惰性气体使容器容积增大
D.保持容器容积不变,充入惰性气体使体系压强增大
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A. 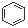 和
和 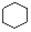 均是芳香烃,
均是芳香烃,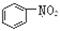 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
B. 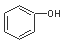 和
和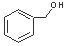 分子组成相差一个—CH2—,因此是同系物关系
分子组成相差一个—CH2—,因此是同系物关系
C.天然气、沼气、坑气、煤气的主要成分都是甲烷
D.分子式为C4H10O的物质,可能属于醇类或醚类
查看答案和解析>>
科目:高中化学 来源: 题型:
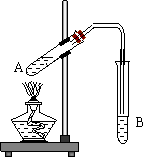
某同学在实验室用下图所示实验装置制取乙酸乙酯。回答下列问题:
(1)在A试管中配制好体积比为3︰2的乙醇和乙酸,加热至沸腾,很
久也未有果香味液体生成,原因是 。
(2)B试管中所装溶液应为 ,乙酸乙酯生成后,将在该溶液
的 (填“上”或“下”) 层,分离出产品所需的玻璃仪器
是 。

查看答案和解析>>
科目:高中化学 来源: 题型:
LiAl/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e-===Li2S+Fe,有关该电池的下列说法中正确的是( )。
A.LiAl在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的电池反应式为:2Li+FeS===Li2S+Fe
C.负极的电极反应式为:Al-3e-===Al3+
D.充电时,阴极发生的电极反应式为:Li2S+Fe-2e-===2Li++FeS
查看答案和解析>>
科目:高中化学 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
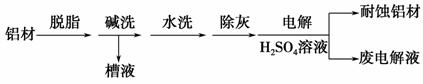
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是_________________________________
(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为_______________________________________________________。
取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是_________________________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是_________________________________________________________________。
(3)利用右图装置,可以模拟铁的电化学防护。
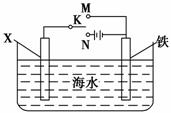
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为______________________________ _____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下面是同学们熟悉的物质:
①CO2 ②金刚石 ③NaBr ④H2SO4 ⑤Na2CO3
⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)属于共价化合物的是________;属于离子化合物的是________。
(2)用电子式表示下列物质的结构
CO2________________;NH4Cl________________;
Na2O________________;NaOH________________。
(2)将NaHSO4溶于水,破坏了NaHSO4中的__________________________,写出其电离方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若不断地升高温度可实现“雪花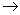 水
水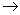 水蒸气
水蒸气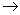 氧气和氢气”的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是( )
氧气和氢气”的变化。在变化的各阶段被破坏的粒子间主要的相互作用依次是( )
A.氢键;分子间作用力;非极性键 B.氢键;氢键;极性键
C.氢键;极性键;分子间作用力 D.分子间作用力;氢键;非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题:
1.写出铬原子的基态的核外电子排布式___________________
2.在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有 (填序号),CS2分子的空间构型是_______ ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
某待测溶液中可能含有SO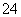 、SO
、SO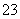 、CO
、CO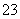 、HCO
、HCO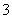 、NO
、NO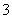 、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出)。
、Cl-、Br-中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出)。
请回答下列问题:
(1)根据上述框图信息填 写下表(不能确定的不填)。
写下表(不能确定的不填)。
| 肯定存在的离子 | 肯定没有的离子 | 沉淀D | |
| 化学式或 离子符号 |
(2)待测溶液中是否有SO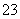 、SO
、SO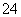 ______________。若气体D遇空气变红色,则生成沉淀D时肯定发生的反应的离子方程式为______________,形成沉淀B时反应的离子方程式为______________。
______________。若气体D遇空气变红色,则生成沉淀D时肯定发生的反应的离子方程式为______________,形成沉淀B时反应的离子方程式为______________。
(3)若Mn+为常见金属阳离子且原子序数不大于20,则要确定它具体是何种离子的方法 是___________________________________________________________________________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com