
|
下列反应离子方程式正确的是 | |
A. |
向氯化铝溶液中加入过量氢氧化钠溶液:Al3++4OH-=[Al(OH)4]- |
B. |
向苯酚钠溶液中通入二氧化碳:CO2+H2O+2C6H5O-→2C6H5OH+CO32- |
C. |
向小苏打溶液中加入醋酸溶液:HCO3-+H+=H2O+CO2↑ |
D. |
向溴化亚铁溶液中通入过量氯气:Fe2++2Br-+2Cl2=Fe3++Br2+4Cl- |
科目:高中化学 来源: 题型:
(10分)X、Y、Z三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42—、OH- |
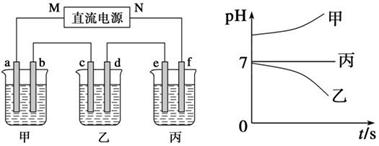
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放250 mL足量的X溶液、足量的Y溶液、足量的Z溶液,电极均为石墨电极。
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的________极(填写“正”或“负”)。
(2)甲烧杯中电极b上发生的电极反应为 。
(3)乙烧杯电解的总反应离子方程式为_________________________________,电解一段时间后停止电解(此时溶液中还有原溶质),若要将乙烧杯中的溶液恢复到原状态,则需要加入 (填化学式)。
(4)若经过一段时间后,丙装置中两极附近均滴酚酞, _______极附近变红,其原因是
。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省金华一中高一下学期期中考试化学试卷(带解析) 题型:填空题
(10分)X、Y、Z三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO42—、OH- |
查看答案和解析>>
科目:高中化学 来源:2014届浙江省高一下学期期中考试化学试卷(解析版) 题型:填空题
(10分)X、Y、Z三种强电解质,它们在水中电离出的离子如下表所示:
|
阳离子 |
Na+、K+、Cu2+ |
|
阴离子 |
SO42—、OH- |
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放250 mL足量的X溶液、足量的Y溶液、足量的Z溶液,电极均为石墨电极。
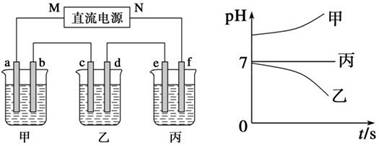
接通电源,经过一段时间后,测得乙中c电极质量增加。常温下各烧杯中溶液的pH与电解时间t的关系图如上。据此回答下列问题:
(1)M为电源的________极(填写“正”或“负”)。
(2)甲烧杯中电极b上发生的电极反应为 。
(3)乙烧杯电解的总反应离子方程式为_________________________________,电解一段时间后停止电解(此时溶液中还有原溶质),若要将乙烧杯中的溶液恢复到原状态,则需要加入 (填化学式)。
(4)若经过一段时间后,丙装置中两极附近均滴酚酞, _______极附近变红,其原因是
。[来源:学_科_网]
查看答案和解析>>
科目:高中化学 来源:2011年山东省实验中学高考化学一模试卷(解析版) 题型:选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com