
分析 8CuFeS2+21O2$\frac{\underline{\;高温\;}}{\;}$SCu+4FeO+2Fe2O3+16SO2中,Cu、O元素的化合价降低,Fe、S元素的化合价升高,由此分析解答.
解答 解:8CuFeS2+21O2$\frac{\underline{\;高温\;}}{\;}$8Cu+4FeO+2Fe2O3+16SO2中,Cu、O元素的化合价降低,Fe、S元素的化合价升高,
①含元素化合价降低的物质被还原,反应中被还原的元素是Cu、O,故答案为:Cu、O;
②由反应可知生成2mol Fe2O3时转移电子的物质的量为4mol×(3-2)+16mol×6=100mol,则生成1mol Fe2O3时转移电子的物质的量为50mol,故答案为:50.
点评 本题考查氧化还原反应,为高频考点,注意把握元素化合价的判断,从化合价变化的角度分析,题目侧重于相关概念的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
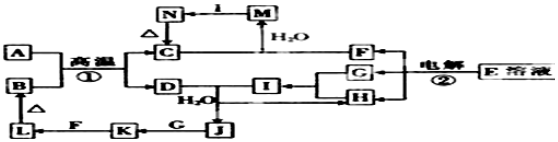
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜作电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑ | |
| B. | Fe3O4与过量的稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向Ba(OH)2溶液中逐滴加入NaHSO4溶液至Ba2+刚好沉淀完全:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | NaHS溶液呈碱性:HS-+H2O?H3O++OH-+S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学性质 | 实际应用 |
| A | 浓硫酸有脱水性 | 浓硫酸作干燥剂 |
| B | Cu能与FeCl3溶液反应 | FeCl3溶液蚀刻铜线路板 |
| C | K2FeO4与水反应生成O2和Fe(OH)3 | K2FeO4可作水的消毒剂和净化剂 |
| D | 常温下干燥的氯气与铁不反应 | 用钢瓶储存液氯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L SO3中含有的分子数为0.5NA | |
| B. | 常温下,46gNO2和N2O4的混合气体中含有原子总数为3NA | |
| C. | 1mol C10H22含共价键数目32NA | |
| D. | 1L 2mol/L的MgCl2溶液中含Mg2+数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01mol•L-1醋酸溶液 | |
| B. | 0.02mol•L-1醋酸与0.02mol•L-1NaOH溶液等体积混合液 | |
| C. | 过量CO2通入到0.01mol•L-1NaOH溶液后所得溶液 | |
| D. | pH=2的盐酸与pH=12的NaOH溶液等体积混合液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验方案 | 所选玻璃仪器 | |
| A | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 | 酒精灯、烧杯、玻 璃棒 |
| B | 证明CH3COOH和HClO的酸性强弱 | 同温下用pH试纸测定浓度为0.1mol•L-1NaClO溶液和0.1mo•L-1 CH3COONa溶液的pH | 玻璃棒、玻璃片 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的银氨溶液,并水浴加热 | 试管、烧杯、酒精 灯、滴管 |
| D | 配制1L 0.1mol•L-1 的CuSO4溶液 | 将25g CuSO4•5H2O溶解在一定量水中,配成1 L溶液 | 烧杯、量筒、玻璃 棒、容量瓶 (1000mL) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
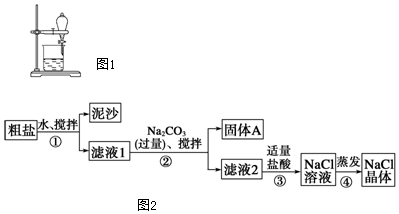
| 猜想 | 验证的方法 | 现象 | 结论 |
| 猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | 有气泡放出,澄清石灰水变浑浊 | 猜想Ⅰ成立 |
| 猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入稀硝酸,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | 猜想Ⅱ不成立 |
| 猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水,滴入BaCl2溶液和稀HNO3溶液 | 有白色沉淀且不溶于稀HNO3 | 猜想Ⅲ成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com