
��֪��2CO��g��+O2��g��=2CO2��g����H=-566kJ��mol-1
Na2O2��s��+CO2��g��=Na2CO3��s��+![]() O2 ��g����H=-226ld��mol-1
O2 ��g����H=-226ld��mol-1
���������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ����
A��CO��ȼ����Ϊ283kJ
B��2Na2O2��s��+2CO2��s��=2Na2CO3��s��+O2��g�� ��H>-452kJ��mol-1
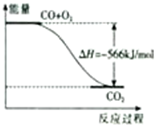
C����ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ
D��CO��g����Na2O2��Ӧ�ų�509kJ����ʱ������ת����Ϊ6.02��1023
 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��֪��2CO��g��+O2��g��=2CO2��g����H=-566kJ/mol2Na2O2��s��+2CO2��g��=2Na2CO3��s��+O2��g����H=-452kJ/mol���������Ȼ�ѧ����ʽ�������жϲ���ȷ���ǣ�������
��֪��2CO��g��+O2��g��=2CO2��g����H=-566kJ/mol2Na2O2��s��+2CO2��g��=2Na2CO3��s��+O2��g����H=-452kJ/mol���������Ȼ�ѧ����ʽ�������жϲ���ȷ���ǣ��������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��+172.5 kJ/mol | B��-172.5 kJ/mol | C��+110.5kJ/mol | D��-110.5kJ/mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com