
| A、v(A)=0.15 mol?L-1?min-1 |
| B、v(B)=0.015 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(D)=0.45 mol?L-1?min-1 |
| v(A) |
| 1 |
| v(B) |
| 3 |
| v(C) |
| 2 |
| v(D) |
| 2 |


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
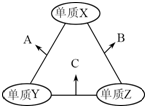 X、Y、Z三种短周期元素,原子半径的大小关系为:r(Y)>r(X)>r(Z),原子序数之和为16.X、Y、Z三种元素的常见单质在适当条件下可发生右图所示变化,其中B和C均为10电子分子.下列说法不正确的是( )
X、Y、Z三种短周期元素,原子半径的大小关系为:r(Y)>r(X)>r(Z),原子序数之和为16.X、Y、Z三种元素的常见单质在适当条件下可发生右图所示变化,其中B和C均为10电子分子.下列说法不正确的是( )| A、X元素位于ⅥA |
| B、A不能溶解于B中 |
| C、B的沸点高于C的沸点 |
| D、A和C不可能发生氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、BaSO4、NaCl、NaHCO3均属于强电解质 |
| B、SO2、NO2、NO均属于二次污染物 |
| C、NaHCO3、NH4Cl、(NH4)2CO3三种固体受热后均无固体剩余 |
| D、FeCl2、NaHSO3、Fe(OH)3都可以通过化合反应直接制得 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水属于非电解质 |
| B、氢氧两种元素只能组成水 |
| C、0℃时冰的密度比液态水的密度大 |
| D、标准状况下,18g水分子的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,28g Fe与足量的浓硝酸反应,转移的电子数为1.5 NA |
| B、常温常压下,4.6 g的NO2和N2O4混合物中,含原子总数为0.3NA |
| C、1.0L 1.0 mol/LNaAlO2水溶液中含有的氧原子数为2NA |
| D、11.2LCl2通入足量氢氧化钠溶液中充分反应,转移的电子数等于0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% |
| B、在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2 NA个电子 |
| C、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| D、一定温度下,1 L 0.50 mol?L-1NH4Cl溶液与2 L 0.25mol?L-1NH4Cl溶液含NH4+物质的量不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
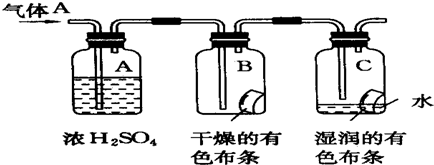
查看答案和解析>>
科目:高中化学 来源: 题型:
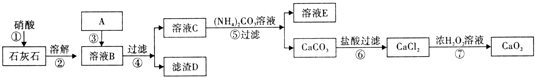
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com