
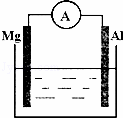
如图所示装置:
(1)若烧杯中溶液为稀硫酸,则观察到的现象为 式为:正极 .该装置将化学能转化为
(2)若烧杯中溶液为氢氧化钠溶液,则负极为 方程式为
考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: Mg比Al活泼,二者都可与酸反应,如电解池溶液为酸,则Mg为负极,发生氧化反应,Al为正极,发生还原反应;
如电解质溶液为碱性,因Mg与碱不反应,而Al反应,则Al为负极,以此可解答该题.
解答: 解:(1)该装置为原电池装置,将化学能转变为电能,镁比铝活泼,当溶液呈酸性时,镁作原电池负极,发生氧化反应,镁逐渐溶解,铝极上有气泡冒出,电流表指针发生偏转,电极反应为Mg﹣2e﹣=Mg2+,铝作正极,发生还原反应,电极反应为2H++2e﹣=H2↑,
故答案为:镁逐渐溶解,铝极上有气泡冒出,电流表指针发生偏转;2H++2e﹣=H2↑;Mg﹣2e﹣=Mg2+;化学;电;
(2)当溶液呈碱性时,铝能与NaOH溶液反应,而镁不反应,所以铝作负极,镁作正极,电池总反应和铝与NaOH溶液的反应相同,为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:Al;2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
点评: 本题考查原电池的组成和工作原理,题目难度不大,注意把握以镁、铝为电极材料,电解质溶液的酸碱性不同,电极反应不同,为易错点.


 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
关于原子轨道的说法正确的是( )
|
| A. | 凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体 |
|
| B. | CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
|
| C. | sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组能量相同的新轨道 |
|
| D. | 凡AB3型的共价化合物,其中心原子A均采用sp3杂化方式成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液体积比为3:2:1时,三种溶液中Cl﹣的物质的量之比为()
A. 1:1:1 B. 1:2:3 C. 3:2:1 D. 3:4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于碱金属的电子结构和性质的叙述中不正确的是()
A. 碱金属原子最外层都只有一个电子,在化学反应中容易失去
B. 都是强还原剂
C. 都能在O2中燃烧生成过氧化物
D. 都能与水反应生成碱
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质,前者属于电解质,后者属于非电解质的是()
A. NaCl晶体、BaSO4 B. 液态的醋酸、酒精
C. 铜、二氧化硫 D. 熔融的KNO3、硫酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
能用H++OH﹣=H2O来表示的化学反应是()
A. Ba(OH)2溶液滴入稀硝酸中
B. NaHSO4溶液和澄清石灰水反应
C. 氢氧化镁和稀盐酸反应
D. 二氧化碳通入NaOH溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式中书写正确的是()
A. 铁和稀硫酸反应:2Fe+6H+═2Fe3++3H2↑
B. 碳酸钙和稀盐酸反应:CaCO3+2H+═Ca2++CO2↑+H2O
C. 铜和硝酸银溶液反应:Cu+Ag+═Cu2++Ag
D. 硫酸镁溶液与氢氧化钡溶液反应:Mg2++2OH﹣═Mg(OH)2↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com