
| A. | 常温常压下,1mol氦气含有的原子数为NA | |
| B. | 常温常压下,8g甲烷中含有的电子数为5NA | |
| C. | 22 g CO2 与标准状况下11.2 L O2含有相同分子数 | |
| D. | 标准状况下,11.2L四氯化碳所含分子数 0.5NA |
分析 A.He是单原子分子,每个分子中含有1个原子;
B.n(CH4)=$\frac{8g}{16g/mol}$=0.5mol,每个甲烷分子中含有10个电子,则8g甲烷中电子的物质的量为5mol;
C.n(CO2 )=$\frac{22g}{44g/mol}$=0.5mol,n(O2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,根据N=nNA计算分子数;
D.标况下,四氯化碳是液体,气体摩尔体积对其不适用.
解答 解:A.A.He是单原子分子,每个分子中含有1个原子,所以1mol氦气含有的原子数为NA,故A正确;
B.n(CH4)=$\frac{8g}{16g/mol}$=0.5mol,每个甲烷分子中含有10个电子,则8g甲烷中电子的物质的量为5mol,8g甲烷中含有的电子数为5NA,故B正确;
C.n(CO2 )=$\frac{22g}{44g/mol}$=0.5mol,n(O2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,根据N=nNA知,分子个数只与物质的量有关,物质的量相同其分子数相同,故C正确;
D.标况下,四氯化碳是液体,气体摩尔体积对其不适用,则无法计算四氯化碳物质的量,导致无法计算其分子数,故D错误;
故选D.
点评 本题考查物质的量有关计算,为高频考点,侧重考查学生分析判断及计算能力,明确分子构成、各个物理量关系是解本题关键,注意气体摩尔体积适用范围和适用条件,易错选项是AD.


科目:高中化学 来源: 题型:实验题
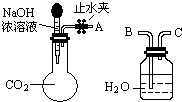 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | 产生白色沉淀 | 有CO32- |
| ②过滤,取2mL滤液于试管中 | ||
| ③滴加酚酞 | 溶液变红 | 有OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 全部可以 | B. | 仅②可以 | C. | 仅②⑤可以 | D. | ①③④可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | S8转化为S6、S4、S2属于物理变化 | |
| B. | 不论哪种硫分子,完全燃烧时都生成SO3 | |
| C. | S8分子中硫原子的杂化方式是sp3杂化 | |
| D. | 把硫单质在空气中加热到750℃即得S2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
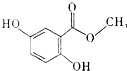
| A. | 分子式为C8H6O4 | |
| B. | 所有的碳原子可能在同一平面内 | |
| C. | 能发生消去反应 | |
| D. | 每摩尔龙胆酸甲酯最多与4molH2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4$\stackrel{高温}{→}$C+2H2 | B. | 2HI+Cl2=2HCl+I2 | ||
| C. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | D. | C2H6+Cl2$\stackrel{光}{→}$C2H5Cl+HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中三个碳原子可能处于同一直线上 | |
| B. | 分子中三个碳原子以单键结合成链状 | |
| C. | C3F8与C3H8互为同分异构体 | |
| D. | 全氟丙烷的电子式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
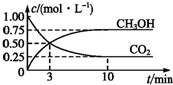 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍关注,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验:在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯能使酸性高锰酸钾溶液和溴水因发生化学反应而褪色 | |
| B. | 不慎把苯酚溶液沾到了皮肤上,应立即用大量水冲洗 | |
| C. | 配制银氨时,应将大量浓氨水一次性加入到少量硝酸银溶液中 | |
| D. | 用银氨溶液或新制氢氧化铜来检验醛或酮时,均只需要水浴加热 | |
| E. | 配制氢氧化铜悬浊液时,应将少量硫酸铜溶液加入到过量的氢氧化钠溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com