
常温下,向一定浓度的醋酸溶液中逐滴加入氢氧化钠溶液直至过量,在此操作过程中,有关溶液中离子浓度变化的大小关系不正确的是 ( )
A.当pH=7时,c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
B.当pH>7时,c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
C.当恰好完全中和时,c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.无论溶液显什么性都有关系:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
对羟基苯甲酸丁酯(俗称尼泊金丁酯)可用作防腐剂,对酵母菌和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得。以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
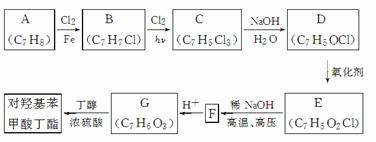
已知以下信息:
①通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基;
②D可与银氨溶液反应生成银镜;
③F的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积比为1∶1。
回答下列问题:
(1)A的化学名称为________;
(2)由B生成C的化学反应方程式为________,该反应的类型为________;
(3)D的结构简式为________;
(4)F的分子式为________;
(5)G的结构简式为________;
(6)E的同分异构体中含有苯环且能发生银镜反应的共有________种,其中核磁共振氢谱有三种不同化学环境的氢,且峰面积比为2∶2∶1的是________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列应用化学科学对物质进行研究的基本方法或所得的结论,不正确的是 ( )
A.焰色反应实验,若火焰呈黄色,不能确认是否含有钾元素
B.根据CO2和SiO2都是酸性氧化物,推知两者物理性质相似
C.根据电解质在水溶液中能否完全电离,将电解质分为强电解质与弱电解质
D.测定物质的量浓度相同的NaA和NaB溶液的PH,可以比较对应酸的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
A~H均为有机化合物,它们之间的转化如下图所示:
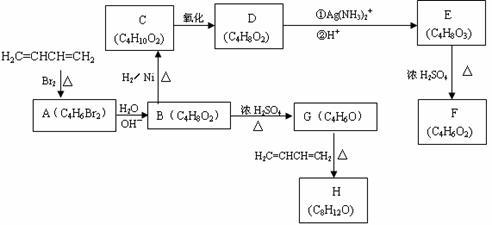
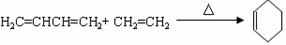 提示:已知反应
提示:已知反应
实验表明:①D既能发生银镜反应,又能与金属钠反应放出氢气;② F不能使溴水褪色;③G能使溴的四氯化碳溶液褪色。
请根据以上信息回答下列问题:
⑴A的结构简式为 ,由A生成B的反应类型是 反应;
⑵D的结构简式为 。
⑶由E生成F的化学方程式为 ,与E具有相同官能团的E的同分异构体还有 (写出结构简式,只要写2个);
⑷G的结构简式为 ;
⑸由G生成H的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
苯酚在一定条件下能与氢气加成得到环己醇。下面关于这两种有机物的叙述中,错误的是( )
A.都能溶于水,但溶解性都比乙醇的差
B.都能与金属钠反应放出氢气
C.苯酚是比碳酸更强的酸,环己醇则显中性
D.苯酚与FeCl3溶液作用显紫色,环乙醇加入FeCl3溶液中无明显现象
查看答案和解析>>
科目:高中化学 来源: 题型:
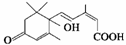
2009年国庆庆典期间,在北京长安街等主要街道上,出现了一座座拔地而起的立体花坛,4 000万盆、上百种鲜花扮靓了北京街头。大量盆栽鲜花因施用了S诱抗素制剂,得以保证鲜花盛开,S诱抗素的分子结构如图,下列关于该分子的说法正确的是( )
A.含有碳碳双键、羟基、羰基、羧基
B.含有苯环、羟基、羰基、羧基
C.含有羟基、羰基、羧基、酯基
D.含有碳碳双键、苯环、羟基、羰基
查看答案和解析>>
科目:高中化学 来源: 题型:
将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一。煤转化为水煤气的主要化学反应为C(s)H2O(g)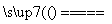 CO(g)+H2(g)。
CO(g)+H2(g)。
C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1
H2(g)+1/2O2(g)===H2O(g) ΔH2=-242.0 kJ·mol-1
CO(g)+1/2O2(g)===CO2(g) ΔH3=-283.0 kJ·mol-1
请回答:
(1)请你根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式:________________________________________________________________________。
(2)比较反应热数据可知,1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量之和,比1 mol C(s)完全燃烧放出的热量________(填“多”或“少”)。
甲同学据此认为:“煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量。”
乙同学根据盖斯定律作出了下列循环图:
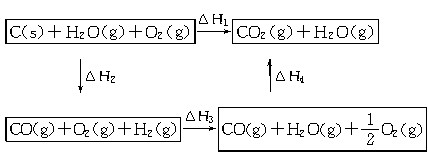
请你写出ΔH1、ΔH2、ΔH3、ΔH4之间存在的关系式__________________________。
乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同。”请分析:甲、乙两同学观点正确的是________(填“甲”或“乙”)同学,另一同学出现错误观点的原因是________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com