
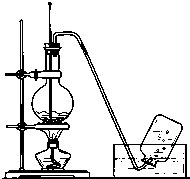
 实验室常用如图所示装置制取乙烯,制取时:
实验室常用如图所示装置制取乙烯,制取时:分析 A、反应药品浓H2SO4(18.4mol/L)与乙醇按3:1的体积比混合;
B、加热液体时为防止液体暴沸,需要加入碎瓷片;
C、乙醇加热到170摄氏度时发生分子内消去生成乙烯,140摄氏度发生分子间取代反应,据此解答即可;
D、98%的浓硫酸具有强氧化性,能氧化乙醇,据此解答即可.
解答 解:A.所用的反应药品为1体积酒精和3体积浓度为18.4mol/L的硫酸,故答案为:1:3;
B、加热液体时为防止液体暴沸,需要加入碎瓷片或沸石,故答案为:沸石;
C、乙醇加热到170℃时发生分子内消去生成乙烯,故答案为:170;
D、实验中,试管内溶液颜色随反应进行逐渐加深,最后变成黑色,黑色为碳,为98%的浓硫酸具有强氧化性,氧化乙醇所致,故答案为:黑;浓硫酸将乙烯碳化生成C单质.
点评 本题考查了乙烯实验室制备的原理和反应条件分析,题目较简单.注意所用硫酸为浓硫酸,浓硫酸具有强氧化性.


科目:高中化学 来源: 题型:选择题
| A. | 充分加热至沸腾 | B. | 加入乙醛太少 | ||
| C. | 加入NaOH溶液的量不够 | D. | 加入CuSO4溶液的量不够 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化产物为Fe3O4和SiO2 | |
| B. | 氧化剂与还原剂物质的量的之比为2:3 | |
| C. | 当有1.5mol Fe2SiO4参加反应时,转移的电子为3 mol | |
| D. | 当有1mol CO2参加反应时,被氧化的Fe2SiO4的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
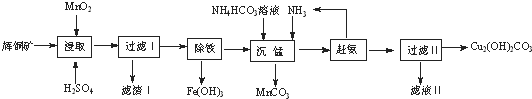
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Mg2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.32 | 25.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
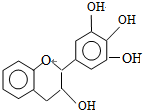
| A. | 分子式为C15H12O5 | |
| B. | 1molEGC与5molNaOH恰好完全反应 | |
| C. | 易发生氧化反应和取代反应,不能发生消去反应 | |
| D. | 遇FeCl3溶液能发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 容器内混合气体的密度不随时间的变化而变化 | |
| B. | 单位时间内每消耗3mol H2,同时生成2mol NH3 | |
| C. | 混合气体的总质量不随时间的变化而变化 | |
| D. | 混合气体的总物质的量不随时间的变化而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
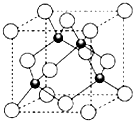 X、Y、Z三元素的原子序数依次增大,三原子的核外最外层电子排布均为4s1.
X、Y、Z三元素的原子序数依次增大,三原子的核外最外层电子排布均为4s1.| r(Zn2+) | r(Z+) | r(S2-) | r(Cl-) | 熔点 | |
| ZnS | ZCl | ||||
| 74pm | 77pm | 184pm | 181pm | 1700℃ | 430℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com