
| A、在铁门上焊接铜块能防腐蚀 |
| B、镀锡铁制品的镀层破损后,镀层仍能对铁制品起保护作用 |
| C、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
| D、在海轮外壳连接锌块,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
 )是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示.
)是一种重要的化工原料和医药中间体,实验室合成三苯甲醇的合成流程如图1所示.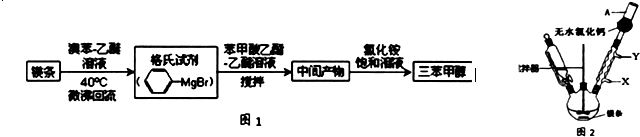
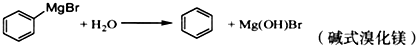
| 物质 | 熔点 | 沸点 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有机溶剂 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、笨等有机溶剂 |
| 溴苯 | -30.7℃ | 156.2℃ | 不溶于水,溶于乙醇、乙醚等多数有机溶剂 |
| 苯甲酸已酯 | -34.6℃ | 212.6℃ | 不溶于水 |
| Mg(OH)Br | 常温下为固体 | 能溶于水,溶于乙醇、醚等多数有机溶剂 | |
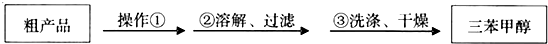
查看答案和解析>>
科目:高中化学 来源: 题型:
A、C=
| ||
B、已知常温下,氨水的电离常数为Ka,则pH约等于14+lg
| ||
| C、上述溶液中再加入0.5VmL同浓度稀盐酸,充分反应后c(Cl-)=c(NH4+)+c(NH3?H2O) | ||
| D、上述溶液中再加入VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室需要0.1mol/L NaOH溶液 250mL.根据这种溶液的配制情况,回答下列问题.
实验室需要0.1mol/L NaOH溶液 250mL.根据这种溶液的配制情况,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在常温下铜与浓硝酸反应,说明硝酸只有氧化性 |
| B、铵盐加热都能分解,但不一都能生成氨气 |
| C、工业上用反应Na+KCl=NaCl+K 制取金属钾,说明钠的还原性强于钾 |
| D、溴中溶有少量的碘,可以用酒精萃取的方法提纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯水加入有色布条,有色布条褪色,说明溶液中有Cl2存在 |
| B、氯水溶液呈黄绿色,有刺激性气味,说明有Cl2存在 |
| C、氯水加入盐酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在 |
| D、氯水加入NaOH溶液,氯水黄绿色消失,说明有HClO存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解AlCl3溶液,在阴极上析出金属Al |
| B、氢氧燃料电池中,氧气是正极反应物 |
| C、用惰性电极电解CuSO4溶液一段时间,溶液酸性不变 |
| D、铅蓄电池在充电时,连接电源正极的电极反应为:PbSO4+2e-═Pb+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、13C与15N具有相同的中子数 |
| B、C60、13C和石墨互为同素异形体 |
| C、等物质的量的13C17O、15N2两种气体具有相同的质子数和原子数 |
| D、13C、15N和C60、N70互为同位素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com