
| A�� | ��֪�к���Ϊ57.3kJ/mol����0.5mol H2SO4��Ũ��Һ�뺬1molNaOH����Һ��ϣ��ų�����Ϊ57.3 kJ | |
| B�� | ��C��ʯī��=C�����ʯ����H=+119kJ/mol����֪��ʯī�Ƚ��ʯ���ȶ� | |
| C�� | ���������������������ֱ���ȫȼ�գ�ǰ�߷ų��������� | |
| D�� | 2g H2��ȫȼ������Һ̬ˮ�ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g��=2 H2O��l����H=-285.8kJ/mol |
���� A����0.5mol H2SO4��Ũ��Һ�뺬1molNaOH����Һ��ϣ�����1molˮ����Ũ����ϡ�ͷ��ȣ�
B����C��ʯī��=C�����ʯ����H=+119kJ/mol����֪ʯī�����ͣ�
C��ͬ��������̬�ȹ�̬�����ߣ�
D.2g H2��ȫȼ������Һ̬ˮ�ų�285.8kJ��������1mol H2��ȫȼ������Һ̬ˮ�ų�285.8kJ������
��� �⣺A����0.5mol H2SO4��Ũ��Һ�뺬1molNaOH����Һ��ϣ�����1molˮ����Ũ����ϡ�ͷ��ȣ�����ȴ���57.3kJ����A����
B����C��ʯī��=C�����ʯ����H=+119kJ/mol����֪ʯī�����ͣ���ʯī�Ƚ��ʯ���ȶ�����B��ȷ��
C��ͬ��������̬�ȹ�̬�����ߣ�����������������������ֱ���ȫȼ�գ���������ͬ��ǰ�߷ų��������࣬��C��ȷ��
D.2g H2��ȫȼ������Һ̬ˮ�ų�285.8kJ��������1mol H2��ȫȼ������Һ̬ˮ�ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽΪH2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-285.8kJ/mol����D����
��ѡBC��
���� ���⿼�鷴Ӧ�����ʱ䣬Ϊ��Ƶ���㣬���շ�Ӧ�������仯��ȼ�������к���Ϊ���ؼ������ط�����Ӧ�������Ŀ��飬ע��ѡ��AΪ�����״��㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C6H5Cl | B�� | CH2=CHCl | C�� | CH3COCl | D�� | CH2Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 2��3-����-2-��ϩ | B�� | �� | ||
| C�� | ���� | D�� | ����� | ||
| E�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4H+C��CH4 | B�� | CuSO4•5H2O$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+5H2O | ||
| C�� | CaO+H2O=Ca��OH��2 | D�� | CO2��g����CO2��s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢܢ� | B�� | �ۢܢݢޢ� | C�� | �ڢۢܢ� | D�� | �٢ۢݢޢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 A��B��C��D��E��F��GΪǰ������Ԫ�أ�A��B���������Ų��ɱ�ʾΪasa��bsbbpb��CԪ�ض�Ӧ�����ǿ����к����������ʣ�D���������������ڲ��������3����E��Dͬ���壬��λ��D����һ���ڣ�F��Eͬ���ڣ����DZ������е縺������Ԫ�أ���̬Gԭ�Ӻ�����������7���ܼ��У��Ҽ۲���Ӿ�Ϊ�����ӣ�
A��B��C��D��E��F��GΪǰ������Ԫ�أ�A��B���������Ų��ɱ�ʾΪasa��bsbbpb��CԪ�ض�Ӧ�����ǿ����к����������ʣ�D���������������ڲ��������3����E��Dͬ���壬��λ��D����һ���ڣ�F��Eͬ���ڣ����DZ������е縺������Ԫ�أ���̬Gԭ�Ӻ�����������7���ܼ��У��Ҽ۲���Ӿ�Ϊ�����ӣ�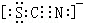 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4NO3 | B�� | NaOH | C�� | MgSO4 | D�� | Na2SO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com