
| A、乙烯的结构简式:CH2CH2 |
B、丙烯的键线式: |
| C、一定条件下,某密闭容器中充入2molSO2(g)和1molO2(g),达到平衡后,放出QkJ热量,则其热化学方程式为:2SO2(g)+O2(g)═2SO3(g )△H=-QkJ?mol-1 |
| D、甲烷的标准燃烧热△H=-890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ?mol-1 |
 ,故B错误;
,故B错误;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、铁粉有剩余,溶液呈浅绿色,Cl-基本保持不变 |
| B、往溶液中滴入无色KSCN溶液,不显红色 |
| C、Fe2+和Fe3+物质的量之比为2:1 |
| D、氧化产物和还原产物的物质的量之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是常温下向20.0mL的盐酸中,逐滴加入0.10mol?L-1NaOH溶液时,溶液的pH随NaOH溶液的体积V(mL)变化的曲线,根据图象所得的下列结论中正确的是( )
如图是常温下向20.0mL的盐酸中,逐滴加入0.10mol?L-1NaOH溶液时,溶液的pH随NaOH溶液的体积V(mL)变化的曲线,根据图象所得的下列结论中正确的是( )| A、原盐酸的浓度为0.10mol?L-1 |
| B、x的值为2.0 |
| C、pH=12,V值为20.4 |
| D、原盐酸的浓度为1.0mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
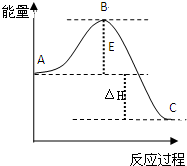 SO2(g)+
SO2(g)+| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com