
【题目】常温下,下列说法正确的是( )
A.pH值都为4的稀盐酸和NH4Cl溶液中,水的电离程度相同
B.浓度均为0.1mol/L的醋酸和NaOH溶液等体积混合后:lg[ ![]() ]=0
]=0
C.在含浓度都为0.01mol/L的Cl﹣、CrO42﹣的混合溶液中滴加AgNO3溶液,先出现沉淀的是AgCl.[已知:Ksp(AgCl)=1.8×10﹣10 , Ksp(Ag2CrO4)=1.9×10﹣12]
D.浓度均为0.1mol/L的NH4Cl和CH3COONH4溶液中,c(NH4+)相同
【答案】C
【解析】解:A.pH值都为4的稀盐酸中水的电离受到抑制,NH4Cl溶液中水的电离受到促进,所以两种溶液中水的电离程度不相同,故A错误; B.0.1mol/L的醋酸中氢离子的浓度小于0.1mol/L,0.1mol/L的NaOH溶液中氢氧根离子浓度等于0.1mol/L,所以lg[ ![]() ]<0,故B错误;
]<0,故B错误;
C.AgCl饱和所需Ag+浓度c(Ag+)= ![]() =
= ![]() =1.8×10﹣8mol/L,
=1.8×10﹣8mol/L,
Ag2CrO4饱和所需Ag+浓度c(Ag+)= ![]() =
= ![]() mol/L=4.36×10﹣5mol/L,则1.8×10﹣8mol/L<4.36×10﹣5mol/L),所以Cl﹣先沉淀,故C正确;
mol/L=4.36×10﹣5mol/L,则1.8×10﹣8mol/L<4.36×10﹣5mol/L),所以Cl﹣先沉淀,故C正确;
D.浓度均为0.1mol/L的NH4Cl和CH3COONH4溶液中,铵根离子水解浓度减小,由于CH3COO﹣水解显碱性,促进铵根离子水解,所以CH3COONH4溶液中,c(NH4+)较小,故D错误.
故选C.


 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:
【题目】(1)某烷烃的相对分子质量为128,其化学式为__________________。
请根据下面给出的有关信息分析该烷烃的分子结构:若该烷烃不能由任何一种烯烃与H2发生加成反应而得到,则该烷烃的结构简式为______________________。
(2)CH3C(CH3)2CH2C(CH3)3系统命名________该烃一氯取代物有________种。
(3)支链只有一个乙基且相对分子质量最小的烷烃的结构简式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁铵[(NH4)2Fe(SO4)26H2O]是分析化学中重要的试剂,学习小组探究其分解产物.
(1)甲组按照图1所示的装置进行实验,关闭止水夹并加热A中的硫酸亚铁铵固体至分解完全,检验其分解产物. 
①装置B仪器名称是 , 所放试剂是 .
②装置C中可观察到的现象是 , 由此可知硫酸亚铁铵的分解产物中有 . (写化学式)
(2)乙组选用甲组实验中的装置A和图2所示的装置进行实验验证硫酸亚铁铵分解的产物中还有SO2和SO3 . ①乙组同学的实验装置中,依次连接的合理顺序(用装置的字母表示)为A、;取适量硫酸亚铁铵固体于A中,通入一段时间N2后,关闭止水夹再点燃酒精灯,通入N2的目的是 .
②装置H中有白色沉淀,则证明分解产物中有;G中发生反应的离子方程式为 .
(3)丙组将一定量的硫酸亚铁铵在500℃时隔绝空气加热一段时间后检验其固体产物,请设计实验证明:此固体产物不含二价铁: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90.取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g.
(1)求该有机物的分子式.
(2)若该有机物呈现酸性,且该有机物的核磁共振氢谱图中出现4个吸收峰,面积比为3:1:1:1,写出其结构简式.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是
4NO(g)+6H2O(g),下列叙述中正确的是
A.达到化学平衡状态时,4v正(O2)= 5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到化学平衡状态
C.达到化学平衡状态后,若增大容器容积,则正反应速率减小,逆反应速率增大
D.化学反应速率的关系为2v正(NH3)= 3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,X,Y分别是直流电源的两极,通电后发现a极板质量增加,b极板处有无色无味的气体放出,符合这一情况的是( ) 
a极板 | b极板 | X电极 | Z | |
A | 锌 | 石墨 | 负极 | CuSO4 |
B | 石墨 | 石墨 | 负极 | NaOH |
C | 银 | 铁 | 正极 | AgNO3 |
D | 铜 | 石墨 | 负极 | CuCl2 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2 mol H2O和2 mol CO置于1 L容器中,在一定条件下,加热至高温,发生如下可逆反应: 2H2O(g)![]()
2H2+O2,2CO+O2![]() 2CO2。
2CO2。
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是________和________,或________和________。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为:n平(O2)= a mol, n平(CO2)=bmol。试求n平(H2O)=________。(用含a、b的代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究碳酸钙与盐酸反应的反应速率,某同学通过如图实验装置测定反应中生成的CO2气体体积,并绘制出如图所示的曲线。请分析讨论以下问题。
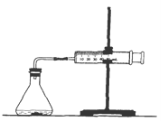
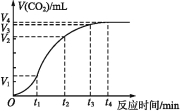
(1)化学反应速率最快的时间段是 ,影响此时间段反应速率的主要因素是 ;
A.O~t1 B.t1~t2 C.t2~t3 D.t3~t4
(2)为了减缓上述反应速率,欲向盐酸中加入下列物质,你认为可行的有 ;
A.蒸馏水 B.NaCl固体 C.NaCl溶液 D.通入HCl
(3)若盐酸的体积是20 mL,图中CO2的体积是标准状况下的体积,则t1~t2时间段平均反应速率v(HCl)= mol·(L·min)-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的水溶液中,加入Ba(OH)2溶液后,原溶液中阴、阳离子个数都减少的是
A. CuSO4 B. Ca(NO3)2 C. Na2CO3 D. FeCl3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com