
【题目】下列不属于“低碳生活”方式的是( )
A. 尽量使用太阳能等代替化石燃料
B. 减少使用一次性筷子
C. 实行数字化办公减少纸张使用
D. 超市购物塑料袋有偿使用
科目:高中化学 来源: 题型:
【题目】利用如图装置进行实验,下列有关实验操作和现象正确的是

A. 缓慢通入N2,再加热Ⅰ处的碳酸氢钠,可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色
B. 缓慢通入N2,加热Ⅰ处KClO3和MnO2的混合物,可观察到Ⅱ处干燥KI淀粉试纸变成蓝色
C. 先对Ⅰ处的氯化铵加热,再缓慢通入N2,可看到Ⅰ处固体减少,Ⅱ处无固体沉积
D. 先缓慢通入CO2,再加热Ⅰ处炭粉,可观察到Ⅱ处氧化铁粉末由红色变成黑色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A的结构简式为 ,下列有关A的说法中正确的是( )
,下列有关A的说法中正确的是( )
A. 常温下,1molA能消耗2molNaOH
B. 1molA与足量的金属钠反应能生成22.4L氢气
C. 1 molA完全燃烧能消耗6molO2
D. A在一定条件下发生酯化反应能生成六元环酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,在100 mL 1 mol·L-1 H2R稀溶液中滴入1 mol·L-1 NaOH溶液,溶液中HR一、R2-的物质的量随pH变化的关系如下图所示。下列有关叙述正确的是

A. pH=4时,溶液中c(HR一)∶c(R2一)=l∶10
B. 滴入150 mL NaOH溶液时,溶液中c(Na+)>c(HR一)>c(R2一)
C. a点溶液中存在c(Na+) +c(H+) =c(HR一)+c(R2一)+c(OH一)
D. c点溶液中含R的微粒有HR-、H2R、R2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高倩同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲把火扑灭,却被实验老师及时制止。原因是CO2可以支持镁燃烧发生以下反应:2Mg+CO2![]() 2MgO+C,下列关于该反应的判断正确的是( )
2MgO+C,下列关于该反应的判断正确的是( )
A. Mg元素化合价由0价升高到+2价,所以MgO是还原产物
B. 由此反应可以判断氧化性CO2>MgO,还原性Mg>C
C. CO2作氧化剂,表现氧化性,发生氧化反应
D. Mg原子失去的电子数目等于氧原子得到的电子数目
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各式表示水解反应的是( )
A.HCO3﹣+H2OH3O++CO32﹣
B.HS﹣+H2OH2S+OH﹣
C.HSO3﹣+H2OSO32﹣+H3O+
D.HCO3﹣+OH﹣H2O+CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】紫菜中含有比较丰富的碘,通常以KI形式存在。KMnO4是强氧化剂,能氧化H2O2、SO32—、Br—、I—、S2—、Fe2+等。某化学兴趣小组拟对市面上销售的某品牌紫菜进行碘的提取和含碘量测定,设计了如下实验步骤:
A.将灼烧后的紫菜灰溶于水,配成悬浊液,过滤
B.将水溶液和试剂甲加入分液漏斗中,震荡后静置,放出下层溶液备用
C.取干燥的紫菜m g于坩埚中灼烧
D.向滤液中滴加少量硫酸酸化的3%的H2O2溶液a ml,充分反应
E.对下层溶液进行某操作,得到碘单质并回收试剂甲
(1)对上述实验步骤进行合理的排序:__________________________________。
(2)步骤D中发生的离子反应为:____________________________________________。
小组中甲同学分析实验时认为步骤D中的H2O2可能有剩余,故取少量酸性高锰酸钾溶液,向其中滴加D中反应后的溶液,若溶液的紫色褪去,则说明H2O2还剩余。小组乙同学认为该结论存在不严谨的地方,请指出你认为不严谨的地方:__________________________
(3)步骤E中“某操作”是_____________。
(4)若实验用的H2O2溶液的密度为1g/cm3,假定所加H2O2溶液恰好完全反应完,则该紫菜中碘的含量可表示为:_______________g/100g(结果不化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.元素周期表中80%左右的非金属元素在现代技术包括能源、功能材料等领城占有极为重要的地位。
(1)氮及其化合物与人类生产、生活息息相关,基态N原子中电子在2p轨道上的排布遵循的原则是_____,N2F2分子中N原子的杂化方式是_______,1mol N2F2含有____个δ键。
(2)高温陶瓷材料Si3N4晶体中N-Si-N的键角大于Si-N-Si的键角,原因是_______。
II.金属元素铁、铜及其化合物在日常生产、生活有着广泛的应用。
(1)铁在元素周期表中的位置_________。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_____(填晶体类型)。Fe(CO)x的中心原子价电子数与配体提供电子吸之和为18,则x=________。
(3)N2是CO的一种等电子体,两者相比较沸点较高的为_______(填化学式)。
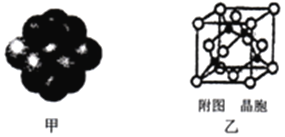
(4)铜晶体中铜原子的堆积方式如下图甲所示。
①基态铜原子的核外电子排布式为___________。
② 每个铜原子周围距离最近的铜原子数目为___________。
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如下图乙所示(黑点代表铜原子)。己知该晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为_________pm。(只写计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com