
| A. | 碱金属原子的最外层电子数都是1,次外层电子数都是8 | |
| B. | 将SO2通入滴有紫色石蕊试液的水中,溶液变成红色 | |
| C. | 白磷易溶于水,不能保存在水中 | |
| D. | 高性能通信材料光 导纤维的主要原料是单品硅 |
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
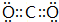 ,②写出B与C形成的化合物C2B的电子式:
,②写出B与C形成的化合物C2B的电子式: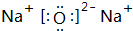 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质:是否只含一种原子 | |
| B. | 氧化还原反应:元素化合价是否变化 | |
| C. | 共价化合物:是否含有共价键 | |
| D. | 强电解质:熔融状态下是否完全电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.8g C2H4和C3H6的混合物中含碳原子数为0.2×6.02×1023 | |
| B. | 在O2参与的反应中,1 mol O2做氧化剂时,得到电子数一定是4×6.02×1023 | |
| C. | 1 L 0.1 mol/L 的Na2S溶液中硫离子数为0.1×6.02×1023 | |
| D. | 标准状况下,11.2 L乙醇中氧原子数为0.5×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol O2和4mol NO2 | B. | 1mol O2和4mol NO | ||
| C. | 1mol NO和5mol NO2 | D. | 4mol NO和1mol NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘酒 | B. | HCl(气态) | C. | 水煤气 | D. | 豆浆 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
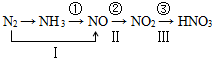
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com