
分析 燃烧反应的方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,由方程式可知,消耗的O2的体积为混合气体体积的$\frac{1}{2}$,由此分析解答.
解答 解:燃烧反应的方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,由方程式可知,消耗的O2的体积为混合气体体积的$\frac{1}{2}$,所以当其完全燃烧时需要O2的体积为$\frac{1}{2}$V L,答:完全燃烧时需要O2的体积$\frac{1}{2}$V L.
点评 本题考查混合物计算、化学方程式有关计算,难度中等,侧重考查学生分析思维能力,注意根据方程式利用方程式找共同的特征,解题就方便了.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④⑤⑩ | B. | ⑥①⑤③ | C. | ⑨②⑧① | D. | ⑦①③⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
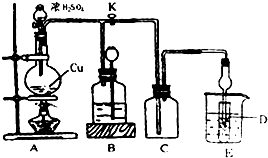
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn为正极 | B. | 负极反应式:O2+4H++4e-→2H2O | ||
| C. | 正极发生氧化反应 | D. | 电解液肯定不是强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com