
| 温度℃ | 700 | 800 | 880 | 1000 | 1200 |
| 平衡常数 | 1.0 | 10.0 | 15.0 | 16.1 | 17.7 |
分析 (1)K为生成物浓度幂之积与反应物浓度幂之积的比,由表格数据可知,温度越高,K越大;
(2)800℃时,K=10.0,初始2mim内A的平均反应速率为0.01mol•L-1•min-1,转化的A为0.02mol/L,则
A(g)+B(g)?C(g)+D(s)
开始 0.08 0.14 0
转化 0.02 0.02 0.02
2min 0.06 0.12 0.02
结合Qc与K的关系判断是否为平衡状态;
(3)结合平衡的特征“等、定”及衍生的物理量判定平衡;
(4)880℃时,互为相反的两个反应的K互为倒数关系.
解答 解:(1)由A(g)+B(g)?C(g)+D(s),纯固体不能代入K的表达式中,K=$\frac{c(C)}{c(A)c(B)}$,由表格数据可知,温度越高,K越大,则正反应为吸热反应,△H>0,
故答案为:$\frac{c(C)}{c(A)c(B)}$;>;
(2)800℃时,K=10.0,初始2mim内A的平均反应速率为0.01mol•L-1•min-1,转化的A为0.02mol/L,则
A(g)+B(g)?C(g)+D(s)
开始 0.08 0.14 0
转化 0.02 0.02 0.02
2min 0.06 0.12 0.02
则2min时c(A)=0.06mol•L-1,C的物质的量为0.02mol/L×5L=0.1mol;此时,Qc=$\frac{0.02}{0.06×0.12}$=2.78<K,该可逆反应没有达到平衡,
故答案为:0.06;0.1;否;
(3)a.该反应为气体体积不等的反应,压强不随时间改变,达到平衡状态,故选;
b.混合气体的质量为变量,则气体的密度不随时间改变,达到平衡状态,故选;
c.单位时间内消耗A和B的物质的量相等,只体现正反应速率关系,不能判定平衡,故不选;
d.C的百分含量保持不变,可知浓度不变,为平衡状态,故选;
故答案为:abd;
(4)880℃时,A(g)+B(g)?C(g)+D(s)反应的平衡常数K=15.0,互为相反的两个反应的K互为倒数关系,则880℃时,反应 C(g)+D(s)?A(g)+B(g)的平衡常数的值为$\frac{1}{15.0}$=0.067,故答案为:0.067.
点评 本题考查化学平衡的计算,为高频考点,把握表中数据、平衡三段法、K的计算、平衡判定为解答的关键,侧重分析与计算能力的考查,注意利用Qc与K的关系判断平衡移动,题目难度中等.


 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲>乙>丙 | B. | 乙>甲>丙 | C. | 丙>甲>乙 | D. | 甲>丙>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].
N2O4(g)已达平衡状态,因反应是放热反应,放置时气体温度下降,平衡向正反应方向移动,NO2浓度降低.[已知2NO2(g)?N2O4(g)在几微秒内即可达到化学平衡].查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强p/100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(CO)/mol | n(H2O)/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A. | 反应在t1 min内的平均速率为v(H2)=$\frac{0.40}{{t}_{1}}$mol•L-1•min-1 | |
| B. | 保持其他条件不变,起始时向容器中充入0.60mol CO和1.20mol H2O,到达平衡时n(CO2)=0.40mol | |
| C. | 保持其他条件不变,向平衡体系中再通入0.20mol H2O(g),△H增大 | |
| D. | 温度升高至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
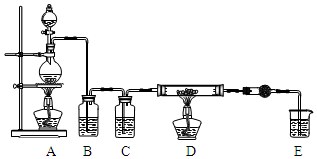 无水AlCl3是一种重要的化工原料.某课外探究小组尝试制取无水AlCl3,查阅资料获得下列信息:无水AlCl3在178℃升华,极易潮解,遇水蒸气产生白色烟雾.
无水AlCl3是一种重要的化工原料.某课外探究小组尝试制取无水AlCl3,查阅资料获得下列信息:无水AlCl3在178℃升华,极易潮解,遇水蒸气产生白色烟雾.| 第一次实验 | 第二次实验 | 第三次实验 | |
| D中固体用量 | 2.0g | 2.0g | 2.0g |
| 氢气的体积 | 334.5mL | 336.0mL | 337.5mL |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com