
【题目】铁是最常见的金属材料。铁能形成[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(III)〕 和Fe(CO)x等多种配合物。
(1)基态Fe3+的核外电子排布式为_____,与NO3-互为等电子体的分子是__________。
(2)尿素(H2NCONH2)分子中C、N原子的杂化方式依次为______。C、N、O三种元素的第一电离能由大到小的顺序是______。
(3)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=______。Fe(CO)x常温下呈液态,熔点为-20 .5 ℃,沸点为103 ℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于_______(填晶体类型)。
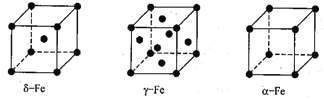
(4)铁有δ、γ、a三种同素异形体,δ、γ、a三种晶胞中铁原子的配位数之比为_______。
【答案】1s22s22p63s23p63d5(或[Ar]3d5)SO3(或BF3)sp2、sp3N>O>C5分子晶体4:6:3
【解析】(1)Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5,3s23p63d5,NO3-中有4个原子,5+6×3+1=24个价电子,SO3中有4个原子,6+6×3=24个价电子,与NO3-是等电子体;
(2)尿素分子中C形成三个σ键,杂化方式为sp2;分子中N原子的价层电子对数为![]() =4,杂化方式为sp3,同一周期元素,元素的第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,C、N、O元素处于同一周期且原子序数逐渐增大,N处于第VA族,所以第一电离能N>O>C,故答案为:N>O>C;
=4,杂化方式为sp3,同一周期元素,元素的第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,C、N、O元素处于同一周期且原子序数逐渐增大,N处于第VA族,所以第一电离能N>O>C,故答案为:N>O>C;
(3)分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5;
(4)δ-Fe为体心立方密堆积,配位数为8,γ-Fe为面心立方密堆积,配位数为12,α=Fe为简单立方堆积,配位数为6,则δ、γ、α三种晶胞中铁原子的配位数之比为8∶12∶6=4∶6∶3。


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】COCl2俗名光气,有毒,在一定条件下,可发生:COCL2(g) ![]() CO(g)+CL2(g) △H<0.下列有关说法正确的是
CO(g)+CL2(g) △H<0.下列有关说法正确的是
A.在一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率
B.当反应达平衡时,恒温恒压条件下通入氨气能提高COCl2的转化率
C.单位时间内生成CO和Cl2的物质的量比为1∶1时,反应达到平衡状态
D.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氨水缓缓地滴入盐酸中至中性,下列有关的说法正确的是
①盐酸过量②氨水过量③恰好完全反应④c(NH4+)=c(Cl-)⑤c(NH4+)<c(Cl-)
A.①⑤ B.③④ C.②⑤ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料。KClO3与浓盐酸发生反应:
KClO3+6HCl(浓)——KCl+3Cl2↑+3H2O
该反应中氧化剂是_____________,还原剂是____________。
被氧化的元素和被还原的元素的质量之比为____________。
转移1mol电子时,产生标准状况下的Cl2____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来可再生能源和清洁能源将成为人类利用新能源的主力军,下列关于能源的叙述正确的是( )
A.化石燃料是可再生能源
B.风能、太阳能是清洁能源
C.化石燃料都是清洁能源
D.氢能是不可再生的清洁能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 石灰石既是制玻璃的原料又是制水泥的原料
B. “大漠孤烟直”描述的是物质升华的过程
C. 高锰酸钾和浓盐酸不能保存在同一药品橱中
D. 可用盐酸酸化的BaCl2溶液检验露置的Na2SO3已变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国营养学会修订颁布的“每日膳食营养素供给量”将硒(Se)列为15种每日膳食营养素之一,提出一个成年人每天对硒的适宜摄入量是50 ~250μg。回答下列有关问题:
(1) Se 原子的价电子排布式为_______,基态78 Se 原子中,核外存在______对自旋方向相反的电子。
(2)碱金属的硒化物溶液能够溶解硒,生成多硒化合物(M2Sex)。如多硒化钠Na2Se8,该物质中,化学键类型是________,Se原子之间形成的空间构型为_________________。
(3)As、S在元素周期表中均与Se 相邻,其氢化物分别是AsH3、H2Se和H2S其氢化物的稳定性强弱顺序为______________________。
(4)SeCl2和BeCl2均为1:2组成的分子,SeCl2中Se的轨道杂化类型是_______,BeCl2中Be的轨道杂化类型是_________________。
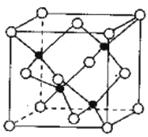
(5)Zn与Se同周期,S与Se同主族。由Zn与S形成的ZnS可用于制白色的颜料及玻璃、发光粉、橡胶、塑料、发光油漆等。ZnS晶胞结构如图所示,黑球代表的原子在晶胞内,白球代表的原子除在顶点外,其余的原子在晶胞_________ (填“内部”“棱上”或“面心”),若该晶体的密度为ρg·㎝-3,阿伏加德罗常数为NA mol-1,则立方晶胞的棱长=_____㎝(用含p、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 氯化钠与浓硫酸混合加热:H2SO4(浓)+2Cl-![]() SO42- + 2HCl↑
SO42- + 2HCl↑
B. 过量的硫化钠溶液与氯化铁溶液反应:2Fe3++S2-=2Fe2++ S↓
C. 碳酸氢铵溶液与足量NaOH溶液混合后加热:NH4++HCO3-+2OH-![]() CO32-+NH3↑+2H2O
CO32-+NH3↑+2H2O
D. 向次氯酸钙溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铍元素及其化合物的性质的推测正确的是( )
A.铍原子的半径大于硼原子的半径
B.相同条件下,单质铍与酸反应比与单质锂与酸反应剧烈
C.氢氧化铍的碱性比氢氧化钙的碱性强
D.单质铍能与冷水剧烈反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com