
| A、CH4--天然气 |
| B、CO2--水煤气 |
| C、CaCO3--石膏粉 |
| D、NaHCO3--苏打粉 |


科目:高中化学 来源: 题型:

| A、a 为电源的负极 | ||||
| B、Fe电极的电极反应是4OH--4e-=2H2O+O2↑ | ||||
| C、通电一段时间后,铁电极附近溶液先变红 | ||||
D、电解饱和食盐水的化学方程式是2NaCl+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
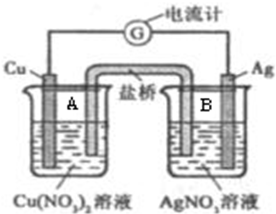 某原电池构造如图所示.其电池的总反应是:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s).请回答以下问题:
某原电池构造如图所示.其电池的总反应是:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s).请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4的摩尔质量是16g |
| B、物质的量是表示含有一定数目粒子集合体的物理量 |
| C、从100mL0.1mol/L盐酸中取出10mL,溶液密度不变 |
| D、4.4gCO2含有0.1mol粒子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com