
分析 ①质子数和中子数只要其一不相同就属于不同核素;元素的种类由质子数决定,质子数不同,元素的种类就不同;
②质子数相同,而中子数不同的原子,互称为同位素,元素的左上角数字表示质量数,左下角数字为质子数,据此分析解答.
解答 解:①H、D、T分别为:11H、21H、31H,属于同种元素的不同核素,质子数和中子数只要其一不相同就属于不同核素:H、D、T、14C、14N、16O分别为一种核素,共6种,
故答案为:6;
②元素的左上角数字表示质量数,左下角数字为质子数,H、D、T分别为:11H、21H、31H,都属于氢元素,质子数相同,而中子数不同,它们互为同位素,14C、14N、左上角数字质量数相同,但分属于不同的元素,所以不能互称为同位素,16O、35Cl2、37Cl2.质量数不相同,且35Cl2、37Cl2,为单质,不可能为同位素,
故答案为:14C、14N.
点评 本题主要考查了核数的种类、元素的种类、同位素的概念以及核外电子数的计算,目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷 | |
| B. | 乙二酸俗称草酸,具有还原性,可以使酸性高锰酸钾溶液褪色 | |
| C. | 银氨溶液和氢氧化铜悬浊液可以较长时间存放 | |
| D. | 油脂在酸性或碱性条件下均可发生水解反应,且产物不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂的水解 | |
| B. | 在一定条件下,苯与浓硝酸反应制取硝基苯 | |
| C. | 乙醛与氢气的反应 | |
| D. | 甲烷与氯气在光照条件下反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | H-H | O=O | H-O |
| 键能(KJ/mol) | 436 | 496 | 463 |
| A. | 242 | B. | -242 | C. | 484 | D. | -484 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
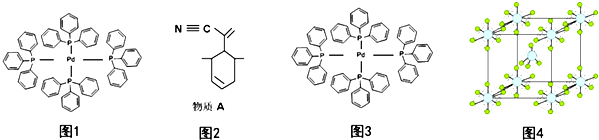
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 空/燃比的增大使氧气的浓度增大,因而CO、CxHy的含量会慢慢变小 | |
| B. | 当空/燃比达到15后由于燃油气含量减少,燃油气燃烧放出的热量相应减少,环境温度降低,故NOx减少 | |
| C. | 空/燃比的增大,燃烧产生的高温及火花塞放电能促使空气中的氮气与氧气直接生成NO2 | |
| D. | 在机动车尾气出口处使用催化剂能将CO、NOx转化为无害的N2和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 2011年9月29日我国成功发射的“天宫一号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分是氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:
2011年9月29日我国成功发射的“天宫一号”飞行器的外壳覆盖了一种新型结构陶瓷材料,其主要成分是氮化硅,该陶瓷材料可由石英固体与焦炭颗粒在高温的氮气流中通过如下反应制得:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
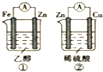
| A. | ①、②装置都能将化学能转化为电能 | |
| B. | ②中的硫酸根离子向负极移动 | |
| C. | ②中的电子轴Zn经过导线流向Cu | |
| D. | ②中铜片上发生的电极反应式为2H++2e-=2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮(
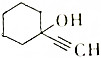
将干燥的乙炔通入液氨中,同时加入钠,并滴加环己酮( 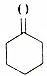 ),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )
),若原料完全反应生成1-乙炔基-1-环己醇,则乙炔与环己酮的质量之比应是( )| A. | 1:1 | B. | 1:2 | C. | 13:49 | D. | 24:49 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com