
���� ��H2O2��O2֪��˫��ˮ�ڷ�Ӧ������ԭ�������Ի��������������μӷ�Ӧ���ڷ�Ӧ�еõ��ӻ��ϼ۽��ͣ����ݻ��ϼ�֪�������������������������ԭ�����������ӣ�ͬʱ��Ӧ������ˮ����Ӧ�����ӷ���ʽΪ2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2����������ӷ���ʽ�����⣮
��� �⣺��1����Ӧ������������H2O2��������Ϊ��ԭ����MnO4-����ԭ����ԭ����ΪMn2+��
�ʴ�Ϊ��H2O2��Mn2+��
��2��������ؾ���ǿ�����ԣ�����������������������Ӧ�������ữ��
�ʴ�Ϊ��ϡ���
��6��2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2����Ӧ�У�MnԪ�ػ��ϼ���+7�۽��͵�+2�ۣ��ɷ���ʽ��֪����5mol����ת��10mol���ӣ����練Ӧת����0.3mo1���ӣ�����������0.15mol�������ڱ�״�������Ϊ0.15mol��22.4L/mol=3.36L��
�ʴ�Ϊ��3.36��
���� ���⿼����������ԭ��Ӧ��������������ԭ��Ӧ�ĸ������ת�Ƶ�֪ʶ�Ŀ��飬��Ŀ�ѶȲ���ע����ݻ��ϼ۵ı仯������


 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2����ʹBr2ˮ��ɫ������ΪSO2����Ư���� | |
| B�� | Na�Ľ������Ա�Mgǿ���ʿ���Na��MgCl2��Һ��Ӧ��Mg | |
| C�� | Fe��Cl2��ȼ������FeCl3����Fe��I2��Ӧ����FeI3 | |
| D�� | ���������Ƶ��������������Ũ��������Ϊ������������Ũ����ۻ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
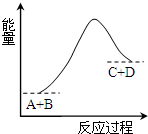
| A�� | �÷�Ӧ��Ӧ��A����������������D������ | |
| B�� | �÷�ӦΪ���ȷ�Ӧ | |
| C�� | ��Ӧ�������������������������� | |
| D�� | �÷�Ӧֻ���ڼ��������²��ܽ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɢ�����Ӳ�������ֽ | B�� | ���ж����ЧӦ | ||
| C�� | ��ɢ�ʺܿ�ͳ������� | D�� | ���÷�ɢϵ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��A��ʾ�ķ�Ӧ������0.4 mol/��L•min�� | |
| B�� | ��B��ʾ�ķ�Ӧ������0.3 mol/��L•min�� | |
| C�� | 2 minĩʱ�ķ�Ӧ���ʣ���B��ʾ��0.3 mol/��L•min�� | |
| D�� | ��D��ʾ�ķ�Ӧ����Ϊ0.1 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
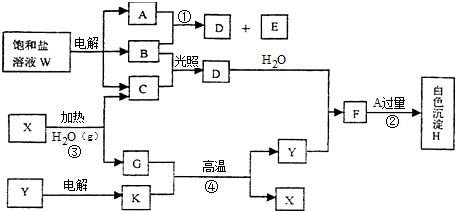
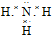 ��B�ľ��������Ƿ��Ӿ��壮
��B�ľ��������Ƿ��Ӿ��壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
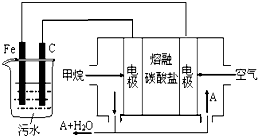
| A�� | FeΪ��������缫��ӦΪ��Fe-3e-+3OH-=Fe��OH��3�� | |
| B�� | ͨ�����ĵ缫Ϊ��������缫��ӦΪ��CH4-8e-+10OH-=CO32-+7H2O | |
| C�� | Ϊ��ʹ��ȼ�ϵ�س�ʱ���ȶ����У���ع���ʱ���� �в���A���ʲμ�ѭ����A������CO2 | |
| D�� | ʵ������У���������������4.48 L���壬���·��ͨ���ĵ��Ӹ���Ϊ0.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ�Ũ��֮��Ϊ2��3��3 | |
| B�� | �ͣ�A�����ͣ�B�����ͣ�C�� ֮��Ϊ2��3��3 | |
| C�� | A��B��C�������ʵ�Ũ�Ȳ���ʱ��仯���仯 | |
| D�� | ���������ʵ���Ũ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com