
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | Na2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | 0.1 mol•L-1 NH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl- |
分析 A.铁离子与硫氰根离子反应生成硫氰化铁;
B.硫化钠与铜离子反应生成硫化铜沉淀;
C.四种离子之间不反应,都不与碳酸氢铵反应;
D.硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子.
解答 解:A.Fe3+和SCN-之间反应生成络合物硫氰化铁,在溶液中不能大量共存,故A错误;
B.Na2S、Cu2+之间反应生成硫化铜沉淀,在溶液中不能大量共存,故B错误;
C.K+、Na+、NO3-、Cl-之间不发生反应,都不与NH4HCO3反应,在溶液中能够大量共存,故C正确;
D.KNO3和NaHSO4的溶液中硝酸根离子能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选C.
点评 本题考查离子共存的判断,为高考的高频题,题目难度不大,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
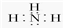 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 14g乙烯和甲烷混合气体中的氢原子数一定大于2NA | |
| B. | 2molN2与6molH2在一定条件下反应生成的NH3 分子数一定大于2NA | |
| C. | 56gFe溶于过量稀硝酸,电子转移数一定等于3NA | |
| D. | 标准状况下,2.24 LCH3Cl含有的共价键数一定小于4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属元素原子最外层电子数越少,该金属失电子能力越强 | |
| B. | 铅位于周期表中金属和非金属的交界处,可作半导体材料 | |
| C. | aA2+、bB+、cC3-三种离子具有相同的电子层结构,则原子序数c>a>b | |
| D. | 若存在简单阴离子R2-,则R一定位于ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子核内有18个中子的氯原子:${\;}_{17}^{35}$Cl | |
| B. | 硫原子的原子结构示意图: | |
| C. | 溴化氢的电子式: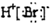 | |
| D. | 乙酸的分子式:CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大理石与醋酸反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+CO2↑+H2O | |
| B. | 硅与NaOH溶液反应:Si+2OH-+H2O═SiO32-+2H2↑ | |
| C. | 水玻璃与醋酸反应:SiO32-+2H+═H2SiO3↓ | |
| D. | 硅石与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com