
【题目】在密闭容器中进行如下化学反应CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表
t/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
请回答下列问题:
(1)该反应的化学平衡常数表达式为:K=________________。
(2)写出一种加快该化学反应的反应速率的方法_____________________。
(3)该反应为_____________反应(填“吸热”或“放热”)。
(4)下列能说明该反应已达到化学平衡状态的是____________________。
a.容器中压强不变 b.混合气体中c(CO)不变
c.υ正(H2)=2υ逆(H2O) d .c(CO2)=c(CO)
(5)某温度下,各物质的平衡浓度符合:c(CO2)c(H2)=c(CO)c(H2O),则该反应的反应温度为_______________________℃。
【答案】![]() 升高温度、增大压强、使用催化剂及增大气体物质的浓度(任选一条) 吸热 b 830
升高温度、增大压强、使用催化剂及增大气体物质的浓度(任选一条) 吸热 b 830
【解析】
(1)根据方程式写化学平衡常数表达式;
(2)升高温度、增大压强、使用催化剂及增大气体物质的浓度,均可增大反应速率;
(3)根据表中数据,升高温度,K增大,平衡正向移动;
(4)a.反应的方程式两边的气体计量数之和相等,则容器中压强始终不变,则压强不变不能判断是否达到平衡状态;
b.反应达到平衡状态时,体系中各量不再改变,则混合气体中c(CO)不变可判断达到平衡状态;
c.υ正(H2)=2υ逆(H2O)时,反应速率方向相反,速率之比不等于化学计量数之比,未达到平衡状态;
d .c(CO2)=c(CO)时,不能判断同一物质的反应速率是否相等,不能判断是否达到平衡状态;
(5)K只与温度有关,根据K判断温度。
(1)根据方程式,化学平衡常数表达式K=![]() ;
;
(2)升高温度、增大压强、使用催化剂及增大气体物质的浓度,均可增大反应速率;
(3)根据表中数据,升高温度,K增大,平衡正向移动,则正反应为吸热反应;
(4)a.反应的方程式两边的气体计量数之和相等,则容器中压强始终不变,则压强不变不能判断是否达到平衡状态;
b.反应达到平衡状态时,体系中各量不再改变,则混合气体中c(CO)不变可判断达到平衡状态;
c.υ正(H2)=2υ逆(H2O)时,反应速率方向相反,速率之比不等于化学计量数之比,未达到平衡状态;
d .c(CO2)=c(CO)时,不能判断同一物质的反应速率是否相等,不能判断是否达到平衡状态;
答案为b;
(5)各物质的平衡浓度符合:c(CO2)c(H2)=c(CO)c(H2O),即该温度下,K=1,K只与温度有关,则该温度为830℃。


科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
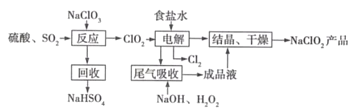
回答下列问题:
(1)NaClO2中Cl的化合价为_______。
(2)写出“反应”步骤中生成ClO2的化学方程式_______。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为________、________。“电解”中阴极反应的主要产物是______。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2。此吸收反应中,氧化剂与还原剂的物质的量之比为________,该反应中氧化产物是_________。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。NaClO2的有效氯含量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H是一种香料,可用如图的设计方案合成。

已知:①在一定条件下,有机物有下列转化关系:
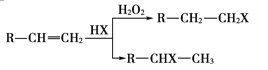 (X为卤素原子)
(X为卤素原子)
②烃A和等物质的量的HCl在不同的条件下发生加成反应,既可以生成只含有一个甲基的B,也可以生成含有两个甲基的F。
(1)D的结构简式为__。
(2)写出D与银氨溶液反应的化学反应方程式___。
(3)A→B和F→G的化学反应类型为___。
(4)E+G→H的化学反应方程式是___。
(5)H有多种同分异构体,其中含有一个羧基,且其烃基上一氯代物有两种的是___(用结构简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10.0mL 0.10 mol·L-1某二元酸H2R溶液中滴加入同物质的量浓度的NaOH溶液,测得溶液的pH随NaOH溶液体积的变化如右图所示。下列说法中正确的是

A. 无法判断H2R是强酸还是弱酸
B. 曲线上m点时溶液中c(Na+)>c(HR-) >c(R2-)>c(H+)
C. HR-的电离能力大于水解能力
D. 溶液中c(Na+)+c(H+)=c(HR-)+c(R2-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 4 molA气体和3molB气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)![]() 2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
2C(g), 若经 2 s后测得 C的浓度为 0.6 molL-1,现有下列几种说法:
①用物质A 表示反应的平均速率为 0.3 molL-1s-1
②物质 B的体积分数是40%
③2 s 时物质 A 的转化率为30%
④2 s 时物质 B 的浓度为 1.0 molL-1
其中正确的是
A.①④B.②③C.①③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质间有如下转化关系,请按要求填空。
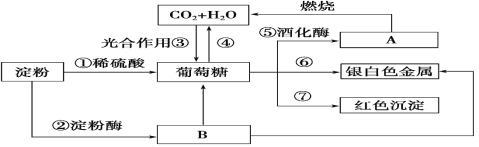
(1)在制镜工业和热水瓶胆镀银时,常利用上述反应________(填序号)。
(2)反应①②的反应类型为_______(填选项字母)。
A.氧化反应 B.加成反应 C.水解反应 D.消去反应
(3)反应⑦可用于检验糖尿病病人尿液中的含糖量,该反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备:

下列叙述错误的是
A. X、Y和Z均能使溴水褪色
B. X和Z均能与NaHCO3溶液反应放出CO2
C. Y既能发生取代反应,也能发生加成反应
D. Y可作加聚反应单体,X可作缩聚反应单体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】南海是一个巨大的资源宝库,开发利用这些资源是科学研究的重要课题。下图为海水资源利用的部分过程,有关说法不正确的是

A.海水淡化的方法主要有蒸馏法、电渗析法、离子交换法
B.氯碱工业中采用阳离子交换膜可提高产品的纯度
C.由MgCl2·6H2O得到无水MgCl2的关键是要在干燥的氯化氢气流低温小火烘干
D.溴工业中③、④的目的是为了富集溴元素,溴元素在反应③、④、⑤中均被氧化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com