
| A、1:1 |
| B、1010:1 |
| C、109:1 |
| D、108:1 |
| C(OH-)氢氧化钠 |
| C(OH-)水 |


科目:高中化学 来源: 题型:
| A、常温下1 mol铜片投入含4 mol HNO3的浓硝酸中 |
| B、常温下1 mol铝片投入足量的浓硫酸中 |
| C、1 mol MnO2粉末与含4 mol HCl的盐酸溶液共热 |
| D、1 mol铜片与含2 mol H2SO4的浓硫酸共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KMnO4酸性溶液和溴的CCl4溶液 |
| B、银氨溶液和溴的CCl4溶液 |
| C、FeCl3溶液和银氨溶液 |
| D、银氨溶液和KMnO4酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质A、B的转化率之比一定是1:2 | ||
B、起始时刻和达平衡后容器中的压强比为(1+n):(1+n-
| ||
| C、若起始放入3molA和3mol B,则达平衡时生成3a mol C | ||
| D、当v正(A)=2v逆(C)时,可断定反应达平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝是较活泼的金属,能跟盐酸、稀硫酸、氢氧化钠溶液反应放出氢气 |
| B、镁铝合金的强度和硬度都比纯铝和纯镁大 |
| C、常温下,铝能和空气里的氧气反应生成一层致密的氧化膜,从而失去光泽 |
| D、镁着火可以用CO2来灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B、淀粉、蛋白质完全水解的产物互为同分异构体 |
| C、乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
| D、石油裂解和油脂皂化都有高分子生成小分子的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
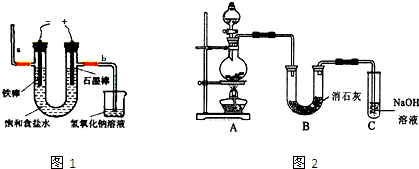
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com