

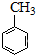
 $→_{水溶加热}^{浓H_{2}SO_{4}浓HNO_{3}}$
$→_{水溶加热}^{浓H_{2}SO_{4}浓HNO_{3}}$
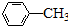 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$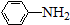 (弱碱性,易被氧化)
(弱碱性,易被氧化) .
. .
. 水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构.
水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构. →B
→B 等.
等. 的同分异构体:
的同分异构体: 、
、 等
等 属于不同类别
属于不同类别 分析 由反应①可知A为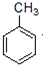 ,反应②为发生取代反应,同时生成HCl,反应③为
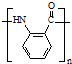
,反应②为发生取代反应,同时生成HCl,反应③为 发生缩聚反应生成高分子化合物
发生缩聚反应生成高分子化合物 .
.
(4)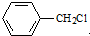 水解产物为
水解产物为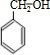 ,其同分异构体遇氯化铁溶液发生显色反,说明含有酚羟基,甲基与酚羟基有邻、间、对三种;
,其同分异构体遇氯化铁溶液发生显色反,说明含有酚羟基,甲基与酚羟基有邻、间、对三种;
(5)由步骤Ⅲ产物结构,可知甲苯发生硝化反应生成T为 ,用高锰酸钾溶液氧化得到J为
,用高锰酸钾溶液氧化得到J为 ,用铁粉和盐酸还原硝基生成
,用铁粉和盐酸还原硝基生成 ;
;
(6)满足以下条件的 的同分异构体:①具有苯环,②与
的同分异构体:①具有苯环,②与 属于不同类别,含有的官能团不都相同,③苯环上的一氯代物只有两种,含有2个不同的取代基且处于对位.
属于不同类别,含有的官能团不都相同,③苯环上的一氯代物只有两种,含有2个不同的取代基且处于对位.
解答 解:由反应①可知A为 ,反应②为发生取代反应,同时生成HCl,反应③为
,反应②为发生取代反应,同时生成HCl,反应③为 发生缩聚反应生成高分子化合物
发生缩聚反应生成高分子化合物 .
.
(1)A为 ,名称为甲苯,故答案为:甲苯;
,名称为甲苯,故答案为:甲苯;
(2)反应②的化学方程式为: ,
,
故答案为: ;
;
(3)反应③为 发生缩聚反应生成高分子化合物B为
发生缩聚反应生成高分子化合物B为 ,
,
故答案为: ;
;
(4)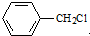 水解产物为
水解产物为 ,其同分异构体遇氯化铁溶液发生显色反,说明含有酚羟基,甲基与酚羟基有邻、间、对三种,结构简式为
,其同分异构体遇氯化铁溶液发生显色反,说明含有酚羟基,甲基与酚羟基有邻、间、对三种,结构简式为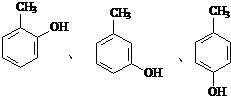 ,
,
故答案为:3;
(5)由步骤Ⅲ产物结构,可知甲苯发生硝化反应生成T为 ,用高锰酸钾溶液氧化得到J为
,用高锰酸钾溶液氧化得到J为 ,用铁粉和盐酸还原硝基生成
,用铁粉和盐酸还原硝基生成 .
.
①T为 ,A→T发生甲基的一硝化反应,如果条件控制不好,还可以发生间位、对位取代反应,可能生成副产物
,A→T发生甲基的一硝化反应,如果条件控制不好,还可以发生间位、对位取代反应,可能生成副产物 等,
等,
故答案为: 等;
等;
②氨基易被氧化,如果先还原硝基生成氨基,后氧化甲基,高锰酸钾会氧化氨基,产生副产物,使产品纯度低,产率低,
故答案为:氨基被氧化,产品含杂质多,产率低;
(6)满足以下条件的 的同分异构体:①具有苯环,②与
的同分异构体:①具有苯环,②与 属于不同类别,含有的官能团不都相同,③苯环上的一氯代物只有两种,含有2个不同的取代基且处于对位,可能的结构简式为:
属于不同类别,含有的官能团不都相同,③苯环上的一氯代物只有两种,含有2个不同的取代基且处于对位,可能的结构简式为: 、
、 等,
等,
故答案为: 、
、 等.
等.
点评 本题考查有机物合成与推断、同分异构体书写、有机反应方程式书写等,注意根据合成路线中有机物的结构进行分析,需要学生熟练掌握官能团的性质与转化,题目难度中等.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:选择题
| A. | 在平衡常数表达式中,反应物浓度用起始浓度表示,生成物浓度用平衡浓度表示 | |
| B. | 平衡常数越大,表示化学反应速率越大 | |
| C. | 可以用化学平衡常数来定量描述化学反应的限度 | |
| D. | 平衡常数的大小与温度、浓度、压强、催化剂有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 熔点/℃ | 沸点/℃ | |
| SiCl4 | -70 | 57.7 | 难溶解NH3和无机盐,在潮湿空气中极易水解 |
| Si3N4 | 1900 | - | 性质稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2与O3互为同位素 | |
| B. | O2与O3的相互转化是物理变化 | |
| C. | 等质量的O2与O3含有相同的质子数 | |
| D. | 在相同的温度与压强条件下,等体积的O2与O3含有相同的原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
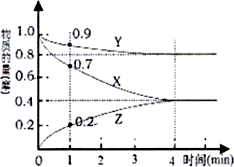 (1)某温度时,在2L的密闭容器在X、Y、Z三种物质的量随时间的变化如图所示.
(1)某温度时,在2L的密闭容器在X、Y、Z三种物质的量随时间的变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn|H2SO4(稀)|C | B. | Cu|CuSO4溶液|Ag | C. | Zn|CCl4|Cu | D. | Fe|H2SO4(稀)|Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | NH4+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1×10-12.如图是向10mLAgNO3溶液中逐滴加入0.1mol•L-1NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )
已知:pAg=-lg[c(Ag+)],Ksp(AgCl)=1×10-12.如图是向10mLAgNO3溶液中逐滴加入0.1mol•L-1NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )| A. | 原AgNO3溶液的物质的量浓度为0.1 mol•L-1 | |
| B. | 图中x点的坐标为(10,6) | |
| C. | 图中x点表示溶液中c(Ag+)=c(Cl-) | |
| D. | 把0.1 mol•L-1的NaCl溶液换成0.1 mol•L-1的NaI溶液,则图象在终点后变为虚线部分 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com