
如图所示,下列实验操作与方法正确的是( )
|
| A. |
| B. |
|
|
| C. |
| D. |
|
考点:
计量仪器及使用方法;夹持仪器;其他仪器及其使用方法.
专题:
化学实验基本操作.
分析:
根据分液漏斗的使用、试管的加热、胶头滴管以及过滤操作的使用方法和操作要领分析.
解答:
解:A.容量瓶使用前需检验是否漏水,检查时一手托住瓶底,另一只手摁住瓶塞,倒转检查,故A正确;
B.用试管加热液体时,液体不能超过试管容积的 ,且用拇指顶住试管夹短柄,故B错误;
,且用拇指顶住试管夹短柄,故B错误;
C.用胶头滴管滴加液体时不能将胶头滴管插入到试管内部,故C错误;
D.过滤时漏斗应紧贴烧杯内壁,故D错误.
故选A.
点评:
本题考查常见仪器的使用和化学基本操作的方法,题目难度不大,注意在学习中加强基础知识的积累.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:
实验室用铅蓄电池进行电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:
负极为Pb+SO42﹣═PbSO4+2e﹣,
正极为PbO2+4H++SO42﹣+2e﹣═PbSO4+2H2O,
今若制得Cl2 0.025mol,这时电池内消耗的H2SO4的物质的量至少是()
A. 0.025 mol B. 0.050 mol C. 0.10 mol D. 0.20 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
铬是人体必需的微量元素,但铬过量会引起污染,危害人体健康。不同价态的铬毒性不一样,六价铬的毒性最大。下列叙述错误的是( )
A.K2Cr2O7可以氧化乙醇,可用来鉴别司机是否酒后驾驶
B.污水中铬一般以Cr3+存在,与水中的溶解氧作用可被还原为六价铬
C.人体内六价铬超标,服用维生素C缓解毒性,说明维生素C具有还原性
D.1 mol 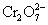 得到6 mol电子时,还原产物是Cr3+
得到6 mol电子时,还原产物是Cr3+
查看答案和解析>>
科目:高中化学 来源: 题型:
关于化学平衡常数的叙述中,正确的是( )
|
| A. | 只与化学反应本身和温度有关 |
|
| B. | 只与反应的温度有关 |
|
| C. | 与化学反应本身和温度有关,并且会受到起始浓度的影响 |
|
| D. | 只与化学反应本身有关,与其他任何条件无关的一个不变的常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
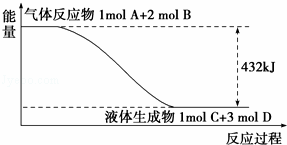
某反应过程中的能量变化如图所示:
(1)写出该反应的热化学方程式:
(2)在溶液中进行化学反应中的物质,其状态标为“aq”,已知0.5mol H2SO4在溶液中与足量氢氧化钠反应放出57.3kJ的热量,用离子方程式写出该反应的热化学方程式: .
(3)合成氨反应的热化学方程式:
N2(g)+3H2(g)⇌2NH3(g)△H=﹣92.2kJ•mol﹣1
已知合成氨反应是一个反应物不能完全转化为生成物的反应,在某一定条件下,N2的转化率仅为10%,要想通过该反应得到92.2kJ的热量,至少在反应混合物中要投放N2的物质的量为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中滴入BaCl2溶液,产生白色沉淀,再滴入稀盐酸,沉淀不溶解,则该溶液中( )
|
| A. | 一定有SO42﹣ | B. | 还可能有CO32﹣ |
|
| C. | 一定无Ag+ | D. | 可能有SO42﹣或Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
I、磷、硫元素的单质和化合物应用广泛。
(1)磷元素的原子结构示意图是____________。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成 白磷,反应为:
白磷,反应为:
2Ca3(PO4)2+6SiO2===6CaSiO3+P4O10 10C+P4O10===P4+10CO
每生成1 mol P4时,就有________mol电子发生转移。
(3)硫代硫酸钠(Na2S2O3)是常用的还原剂。在维生素C(化学式C6H8O6)的水溶液中加入过量I2溶液,使维生素C完全氧化,剩余的I2用Na2S2O3溶液滴定,可测定溶液中维生素C的含量。发生的反应为:
C6H8O6+I2===C6H6O6+2H++2I- 2S2O32-+I2===S4O62-+2I-
在一定体积的某维生素C溶液中加入a mol·L-1 I2溶液V1 mL,充分反应后,用Na2S2O3溶液滴定剩余的I2,消耗b mol·L-1 Na2S2O3溶液V2 mL。该溶液中维生素C的物质的量是__________mol。
(4)在酸性溶液中,碘酸钾(KIO3)和亚硫酸钠可发生如下反应:2IO3-+5SO32-+2H+===I2+5SO42-+H2O
生成的碘可以用淀粉溶液检验,根据反应溶液出现蓝色所需的时间来衡量该反应的速率。某同学设计实验如下表所示:
| 0.01mol·L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol·L-1Na2SO3溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
该实验的目的是_____________________;表中V2=___________mL
II、稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位。
(5)铈(Ce)是地壳中含量最高的稀土元素。在加热条件下CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是______________。
(6)在某强酸性混合稀土溶液中加入H2O2,调节pH≈3,Ce3+通过下列反应形成Ce(OH)4沉淀得以分离。完成反应的离子方程式:
□Ce3++□H2O2+□H2O === □Ce(OH)4↓+□_______
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com