
【题目】下列各组离子中,能在溶液中大量共存的是( )
A.H+ Na+ CO32﹣ Cl﹣
B.Ba2+ Na+Cl﹣ SO42﹣
C.K+ H+ SO42﹣OH﹣
D.Ag+ Al3+ NO3﹣H+
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】一定温度下的恒容密闭容器中,反应A2(g)+B2(g)![]() 2AB(g)达到平衡的标志是
2AB(g)达到平衡的标志是
A. 每断裂1molA-A键,同时也断裂1molB-B键
B. 浓度之比c(A2): c(B2): c(AB)=1:1:2
C. 各物质的浓度不再改变
D. 当混合物的密度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境监测显示,某地市的主要气体污染物为SO2,NOx,CO等,其主要来源为燃煤、机动车尾气。进行如下研究:
(1)为减少燃煤对SO2的排放,可将煤转化为清洁燃料水煤气(CO和H2)。
已知:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ/mol
C(s)+1/2O2(g)=CO(g)△H=-110.5kJ/mol
写出焦炭与水蒸气反应的热化学方程式______;
(2)汽车尾气中NO是在发动机气缸中生成的,反成为:N 2(g)+O 2(g) ![]() 2NO(g) △H>0
2NO(g) △H>0
①将含0.8 mol N2和0.2molO2(近似空气组成)的混合气体充入某密闭容器中,保持1300℃反应达到平衡,测得生成8×10-4molNO 。计算该温度下此反应的化学平衡常数K=_______(填近似计算结果)。
②汽车启动后,汽缸内温度越高,单位时问内NO排放最越大,原因是______________。
(3)利用如图所示装置(电极均为惰性电极)可吸收SO2,并利用阴极排出的溶液吸收NO2。

①电极A的电极反应式为________________;电极B的电极反应式为_____________。
②碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时生成SO32-。该反应的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用三室式电解池(装置结构如图所示,电极均为惰性电极)可以实现用硫酸钠溶液制取硫酸和氢氧化钠。下列叙述正确的是
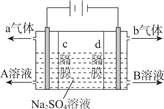
A. a气体为氢气,b气体为氧气
B. A为氢氧化钠溶液,B为硫酸溶液
C. 通电后中问隔室的SO42-向阴极迁移,阳极区溶液的pH增大
D. 该电解反应的方程式为2Na2SO4+6H2O![]() 2H2SO4+4NaOH+O2↑+2H2↑
2H2SO4+4NaOH+O2↑+2H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A→C分两步进行:①A→B,②B→C。反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能)。下列说法正确的是
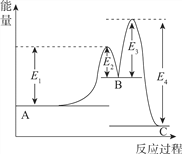
A. 两步反应的ΔH均大于0 B. 加入催化剂能改变反应的焓变
C. 三种物质中C最稳定 D. A→C反应的ΔH=E4-E1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将5.6 g Fe全部溶于200 mL一定浓度的硝酸溶液中,得到标准状况下的气体2.24 L(该气体可能为NO或NO2或NO和NO2的混合气体),又测得反应后溶液中H+的物质的量浓度为0.2 mol·L-1(设反应前后溶液体积的变化忽略不计)。下列说法正确的是( )
A. 2.24 L气体是NO和NO2的混合气体
B. 反应后的溶液中含有Fe2+和Fe3+
C. 反应后的溶液中c(NO![]() )=1.5 mol·L-1
)=1.5 mol·L-1
D. 反应后的溶液最多还能再溶解3.64 g Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 良好的生态环境可以提升生活质量。
① 下列物质不属于空气质量周报中污染物的是________(填字母)。
a. SO2 b. NO2 c. PM2.5
② 垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有________(填字母)标志的垃圾桶内。

③ 燃烧煤产生的SO2所形成的酸雨中,SO2最终转化成的酸是________(填化学式)。
(2) 右图是某品牌调料标签的一部分。

① 配料中的大量氨基酸态氮来源于黄豆中的蛋白质发生________反应得到。
② 小麦粉中的主要营养物质是________。
③ 配料表中属于防腐剂的是________。
④ 配料表中的辣椒红是着色剂。亚硝酸钠也可作着色剂,但亚硝酸钠有毒,要严格控制其用量。亚硝酸钠外观和咸味与食盐很相似,因此要防止因误食亚硝酸钠而发生事故。亚硝酸钠和氯化钠的部分性质如下表:
性质 | 亚硝酸钠 | 氯化钠 |
1. 酸性条件下的稳定性 | 微热分解为NO和NO2 | 微热时不分解 |
2. 熔点 | 271 ℃ | 801 ℃ |
3. 室温时的溶解度 | 约80 g | 约35 g |
请根据表中信息设计一种鉴别NaNO2和NaCl的方法,写出简单的操作过程、现象和结论:________。
(3) 材料是人类赖以生存和发展的重要物质基础。
① 钢铁是应用广泛的金属材料。钢铁在潮湿空气中易生锈,铁锈的主要成分是____________(填化学式),请列举一种防止钢铁腐蚀的方法:________。
② 水泥、玻璃、陶瓷是生活中常见的硅酸盐材料。制备普通玻璃的原料有CaCO3、________和________(填化学式)。青瓷是中国最早发明的瓷器,青瓷表面的绿色是釉层中的________价铁元素显色而成的。
③ 氮化硅陶瓷抗腐蚀能力强,工业上可用四氯化硅和氮气在氢气气氛中加强热发生反应制得。请写出该反应的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的两份铝分别放入过量盐酸和氢氧化钠溶液中,放出的氢气在相同状况下的体积比 ( )
A. 1:1 B. 1:6 C. 2:3 D. 3:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com