
【题目】现有A、B、C、D四种短周期主族元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子均为10电子粒子,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图所示。
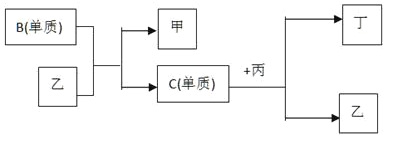
(1)根据以上条件可以确定A、B、C、D四种元素中的三种元素。不能被确定的第四种元素是____(填A、B、C、D中的一种)。
(2)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应;②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙=乙+丁的化学方程式:___________。
(3)NH3H2O的电离方程式为NH3H2O![]() NH4++OH-,试判断NH3溶于水后形成的NH3H2O的合理结构 ________(填字母代号)。
NH4++OH-,试判断NH3溶于水后形成的NH3H2O的合理结构 ________(填字母代号)。

【答案】D 4NH3+5O2![]() 4NO+6H2O (b)
4NO+6H2O (b)
【解析】
A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子粒子,C、D结合生成化合物丁。乙和B单质反应生成C单质和化合物甲,反应是置换反应,因为甲、乙、丙所含质子数相同,则可初步确定A是氢元素。由B可置换C,可确定B是氟元素,C是氧元素,所以D应该是碳元素或氮元素。如果确定B是氯元素,C是硫元素,则D为磷元素或硅元素。这与“C、D两元素形成丁”和“C单质与丙反应生成丁和乙”矛盾。故A是H元素,B是F元素,C是O元素,D是N或C元素。甲是HF,乙是H2O,丙是NH3或CH4,丁是NO或CO2。
(1)根据分析,A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙均为10电子粒子,C、D结合生成化合物丁。乙和B单质反应生成C单质和化合物甲,反应是置换反应,因为甲、乙、丙所含质子数相同,则可初步确定A是氢元素。由B可置换C,可确定B是氟元素,C是氧元素,所以D应该是碳元素或氮元素。如果确定B是氯元素,C是硫元素,则D为磷元素或硅元素。这与“C、D两元素形成丁”和“C单质与丙反应生成丁和乙”矛盾。故A是H元素,B是F元素,C是O元素,D是N或C元素。所以D元素不能确定;
(2) 甲与丙的反应,为HF与NH3的反应,乙与丙的反应为氨气与水的反应,则丙为NH3。反应为4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(3)NH3·H2O电离生成NH4+和OH-,则H2O的氢应与N相连,才能够电离出NH4+;所以合理的图为b。


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】用惰性电极电解法制备硼酸[H3BO3或B(OH) 3]的工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。下列有关说法正确的是( )
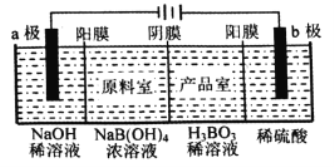
A. 阴极与阳极产生的气体体积比为1:2 B. b极的电极反应式为2H2O-2eˉ=O2↑+4H+
C. 产品室中发生的反应是B(OH)3+OHˉ=B(OH)4ˉ D. 每增加1 mol H3BO3产品,NaOH溶液增重22g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碳酸钠和碳酸氢钠的混合物跟足量盐酸反应,消耗H+和产生CO2的物质的量之比为5:4,该混合物中碳酸钠和碳酸氢钠的物质的量之比为
A.1:3B.2:3C.3:4D.4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如图所示(部分物质与条件己略去)。已知A、C是由两种相同元素组成的物质,其中A的摩尓质量为65g·mol-1,C是白色粉末且焰色反应呈黄色,I是最常见的液体,E是一种红棕色气体,B、F都是无色气体单质。请回答下列问题:

(1)K的电子式为:___________________________。
(2)E的化学式为:___________________________。
(3)写出反应①的化学方程式:___________________________。
(4)写出反应②的离子方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0 g CH4完全燃烧生成液态水放出444.8 kJ热量。则CH4 (g)+2O2(g)=CO2(g)+2H2O(l) ΔH=____________kJ·mol-1。
(2)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向。
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示,则该反应的最佳温度应控制在 ___________左右。
②该反应催化剂的有效成分为偏铝酸亚铜 (CuAlO2,难溶物)。将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为 _____________________。

(3)CH4还原法是处理NOx气体的一种方法。已知一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96 L CH4可处理22.4 L NOx,则x值为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组通过如图所示的流程来制取少量亚硝酸钠晶体(NaNO2),并对其进行纯度测定和相关性质的实验。

已知:Ⅰ.Na2CO3 + NO + NO2 = 2NaNO2 + CO2;
Na2CO3 + 2NO2 = NaNO2 + NaNO3 + CO2
Ⅱ.NaNO2是白色固体,易被氧化。
(1)“还原”步骤中被还原的元素是________。此时SO2从底部通入,硝酸从顶部以雾状喷下,其目的是______。
(2)若使“吸收”步骤中NOX完全转化为NaNO2,则理论上“还原”步骤中SO2与HNO3的物质的量之比为_____。
(3)该课外兴趣小组对实验制取的NaNO2晶体进行纯度测定:
a.称取2.000 g样品,将其配成250 mL溶液。
b.先向锥形瓶内加入40.00 mL 0.100 mol·L-1的H2SO4溶液,加热至40~50℃。冷却后再向其中加入20.00 mL 0. 100 mol·L-1 KMnO4溶液,充分混合。
c.最后用待测的样品溶液与之恰好完全反应,重复三次,平均消耗样品溶液50.00 mL。(NaNO2与KMnO4反应的关系式为:2KMnO4~5NaNO2)
①整个测定过程中应迅速操作,不宜耗时过长,否则样品的纯度____(“偏大”、“偏小”或“无影响”),原因是_______。
②通过计算,该样品中NaNO2的质量分数是_____,可能含有的杂质有________(写出其中两种)。
(4)该课外兴趣小组将NaNO2溶液逐滴加入到含淀粉KI的酸性溶液中,溶液变蓝,同时放出NO气体,该反应的离子方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天飞机用的铝粉与高氯酸铵(NH4ClO4)的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4 ![]() N2↑+ 4H2O+Cl2↑+2O2↑,放出热量为Q,下列对此反应叙述中错误的是( )
N2↑+ 4H2O+Cl2↑+2O2↑,放出热量为Q,下列对此反应叙述中错误的是( )
A. 上述反应瞬间产生大量高温气体推动航天飞机飞行
B. 反应属于分解反应
C. 反应从能量变化上说,主要是化学能转变为热能和动能
D. 在反应中高氯酸铵只起氧化剂作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示。下列说法正确的是

A. 去甲肾上腺素能与乙二酸发生缩聚反应且有多种缩合的可能
B. 每个去甲肾上腺素分子中含有2个手性碳原子(连有四个不同的原子或原子团的碳原子称为手性碳原子)
C. 1mol去甲肾上腺素最多能与2 molBr2发生取代反应
D. 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应故属于氨基酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com