
下列实验操作正确且能达到目的的是( )
A.将AlCl3溶液蒸干得到无水AlCl3
B.在温水瓶中加入Na2CO3溶液浸泡后再加入盐酸除去内壁水垢CaSO4
C.用饱和的NaOH热溶液除去乙酸乙酯中的乙醇、乙酸
D.将Cl2、HCl混合气体通过盛有NaHCO3饱和溶液的洗气瓶除去HCl
科目:高中化学 来源:2014高考化学名师知识点精编 专题6原子结构化学键练习卷(解析版) 题型:选择题
日本大地震引发的福岛第一核电站核泄漏事故,造成放射性物质碘和铯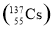 向外界泄漏。下列相关说法错误的是( )
向外界泄漏。下列相关说法错误的是( )
A.每个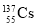 原子中有82个中子
原子中有82个中子
B.CsOH的碱性比KOH强
C.KIO3是碘的最高价氧化物的水化物的盐
D.I-比F-还原性强
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题3离子反应练习卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.显蓝色的淀粉溶液中通入足量SO2后变成无色溶液:I2+SO2+2H2O 2I-+SO42—+4H+
2I-+SO42—+4H+
B.已知电离平衡常数:H2CO3>HClO>HCO32—,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O 2HClO+CO42—
2HClO+CO42—
C.NH4HCO3溶液与过量NaOH溶液反应:NH4++OH- NH3↑+H2O
NH3↑+H2O
D.FeI2溶液中通入过量Cl2:2Fe2++2I-+2Cl2 2Fe3++I2+4Cl-
2Fe3++I2+4Cl-
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题23实验方案的设计与评价练习卷(解析版) 题型:选择题
下列实验装置不能达到实验目的的是( )
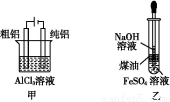
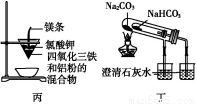
A.甲装置电解精炼铝
B.乙装置制备Fe(OH)2
C.丙装置可得到金属铁
D.丁装置验证NaHCO3和Na2CO3的热稳定性
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题22物质的检验、分离和提纯练习卷(解析版) 题型:选择题
某无色溶液中含有K+、Cl-、OH-、S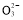 、S
、S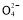 ,为了检验除OH-外的其他所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氢氧化钡溶液、溴水和酚酞六种试剂,设计如下实验步骤,并记录相关现象:
,为了检验除OH-外的其他所有阴离子,拟用盐酸、硝酸、硝酸银溶液、氢氧化钡溶液、溴水和酚酞六种试剂,设计如下实验步骤,并记录相关现象:
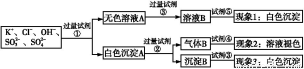
下列有关结论错误的是( )
A.试剂③是AgNO3溶液,试剂⑤是HNO3,现象1中白色沉淀是AgCl
B.现象3中白色沉淀是BaSO4
C.试剂②是盐酸,试剂③是硝酸
D.产生现象2的离子方程式是:Br2+2H2O+SO2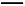 4H++2Br-+S
4H++2Br-+S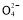
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题21化学实验基础练习卷(解析版) 题型:实验题
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中Na2CO3的质量分数。
【方案一】 称取一定质量的固体样品,通过加热至恒重后冷却,称量剩余固体质量,计算。
(1)下列仪器中,在灼烧固体样品时必须用到的是 (填名称)。

(2)实验中需加热至恒重的目的是: 。
(3)实验中确定加热至恒重的方法是: 。
(4)若加热过程中有晶体迸溅出来,则测得的结果 (填“偏大”、“偏小”或“不变”)。
【方案二】 称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤,干燥沉淀,称量固体质量,计算。
(已知:Ba2++OH-+HC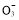
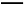 BaCO3↓+H2O)
BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为 。
(2)实验中判断沉淀是否完全的方法是 。
(3)实验中洗涤沉淀的操作是 。
(4)实验中判断沉淀是否洗涤干净的方法是 。
【方案三】 按如图所示装置进行实验:

(1)B装置内所盛试剂是 ;D装置的作用是 ;分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.9 g样品,实验后测得C装置增重8.8 g,则样品中Na2CO3的质量分数为 。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷是 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题21化学实验基础练习卷(解析版) 题型:选择题
下列装置不能完成的实验是( )
ABCD
装
置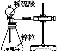
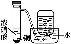

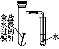
实
验结合秒表粗略测量锌与硫酸的反应速率制备并收集少量NO气体验证温度对化学平衡的影响铁的析氢腐蚀实验
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题1物质的分类分散系练习卷(解析版) 题型:选择题
将淀粉与氯化钾混合液装在半透膜中,浸泡在装有蒸馏水的烧杯中,过一段时间后,取烧杯中液体进行实验,能证明半透膜有破损的是( )
A.加入碘水变蓝色
B.加入硝酸银溶液不产生白色沉淀
C.加入硝酸银溶液产生白色沉淀
D.加入碘水不变色
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题16硫及其化合物练习卷(解析版) 题型:填空题
Na2S2O3·5H2O 俗称“海波”,是常用的脱氧剂、定影剂和还原剂;它是无色易溶于水的晶体,不溶于乙醇,在20 ℃ 和70 ℃ 时的溶解度分别为60.0 g 和212 g,Na2S2O3·5H2O于40~45 ℃熔化,48 ℃分解。下面是实验室制备及相关性质实验。
制备海波的反应原理:Na2SO3+S Na2S2O3
Na2S2O3
制备海波的流程:
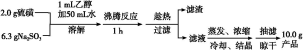
(1)实验开始时用1 mL乙醇润湿硫粉的作用是 。
A.有利于亚硫酸钠与硫磺的充分接触
B.防止亚硫酸钠溶解
C.控制溶液的pH
D.提高产品的纯度
(2)趁热过滤的原因是 。
(3)滤液不采用直接蒸发结晶的可能原因是 。
(4)抽滤过程中需要洗涤产品晶体,下列液体最适合的是 。
A.无水乙醇 B.饱和NaCl溶液 C.水 D.滤液
(5)产品的纯度测定:取所得产品10.0 g,配成500 mL溶液,再从中取出25 mL溶液于锥形瓶中,滴加几滴淀粉作指示剂,然后用0.050 mol/L的标准碘水溶液滴定,重复三次,平均消耗20 mL标准碘水,涉及的滴定反应方程式为:I2+2Na2S2O3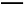 2NaI+Na2S4O6。产品中的Na2S2O3·5H2O的纯度为 %。
2NaI+Na2S4O6。产品中的Na2S2O3·5H2O的纯度为 %。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com