
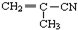 ②
②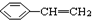 ③
③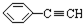 ④CH3-CH=CH-CN ⑤CH2=CH-CH=CH2,其中可用于合成高分子材料(结构如图所示)的正确组合为( )
④CH3-CH=CH-CN ⑤CH2=CH-CH=CH2,其中可用于合成高分子材料(结构如图所示)的正确组合为( )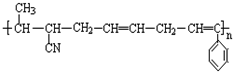
| A. | ①②④ | B. | ①②⑤ | C. | ②④⑤ | D. | ③④⑤ |
分析 解答此类题目,首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断,
加聚产物的单体推断方法:
(1)凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可;
(2)凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可;
(3)凡链节主链上只有碳原子并存在碳碳双键结构的高聚物,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换.
解答 解:该高聚物链节主链不含杂原子,属于加聚反应生成的高聚物,链节主链上存在碳碳双键结构,有8个碳原子,且中间含有1个碳碳双键,其单体必为3种,按如图所示划线断开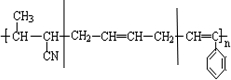 ,在将双键中的1个C-C打开,然后将半键闭合即可的该高聚物单体是:CH3-CH=CH-CN、CH2=CH-CH=CH2、
,在将双键中的1个C-C打开,然后将半键闭合即可的该高聚物单体是:CH3-CH=CH-CN、CH2=CH-CH=CH2、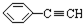 ,即:③④⑤,
,即:③④⑤,
故选D.
点评 本题主要考查不饱和烃加聚反应的规律,题目难度中等,注意掌握根据高聚物判断其单体的方法,明确加成反应原理为解答关键,试题培养了学生灵活应用能力.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:选择题
| A. | 原子最外层电子数:X>Y>Z | B. | 原子序数:X>Y>Z | ||
| C. | 单质沸点:Z>Y>X | D. | 离子半径:X2->Y+>Z- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

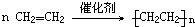 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的电子式: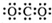 | B. | Cl-的结构示意图: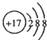 | ||
| C. | 乙醇的结构式:CH3CH2OH | D. | 乙烯的结构简式:CH2CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
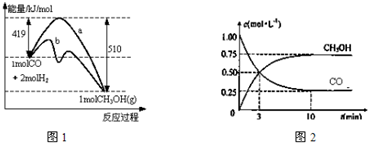
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
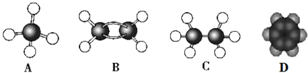
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
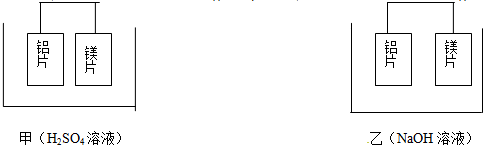
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤③ | B. | ②③④③ | C. | ②③⑤③ | D. | ①③⑤③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com