
科目:高中化学 来源: 题型:解答题
| 实验组别 | 甲 | 乙 | 丙 |
| 稀盐酸的体积(mL) | 50.0 | 50.0 | 50.0 |
| A样品质量(g) | 2.84 | 5.25 | 7.00 |
| 气体的体积(L) | 0.672 | 0.896 | 0.896 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
 Al(OH)3+3H+
Al(OH)3+3H+查看答案和解析>>
科目:高中化学 来源: 题型:多选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
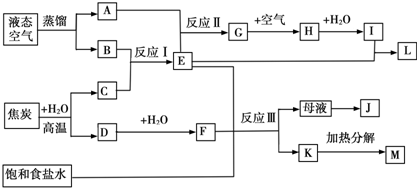
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
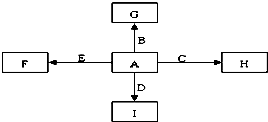 A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知: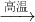 B+H能放出大量的热,该反应曾应用于铁轨的焊接;
B+H能放出大量的热,该反应曾应用于铁轨的焊接; 2F+D,F中的E元素的质量分数为60%.回答问题:
2F+D,F中的E元素的质量分数为60%.回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com