
【题目】常温下,下列说法不正确的是( )
A.0.1mol/L的FeCl3溶液与0.01mol/L的FeCl3溶液中,Fe3+的浓度之比大于10
B.将a mol·L-1的氨水与0.01mol·L-1的盐酸等体积混合后,c(NH4+)=c(Cl-),则NH3·H2O的电离常数为![]()
C.pH加和为12的强酸与弱酸混合,pH可能为6
D.0.1mol·L-1 NH4HS溶液中有:c(NH4+)=c(HS-)+c(S2-)+c(H2S)
【答案】D
【解析】
A、FeCl3在水溶液中能发生水解Fe3+ +3H2O![]() Fe(OH)3+3H+,溶液越稀水解程度越大, Fe3+浓度越小,所以0.01mol/L FeCl3溶液中Fe3+浓度小于0.1mo/L FeCl3溶液中Fe3+浓度的
Fe(OH)3+3H+,溶液越稀水解程度越大, Fe3+浓度越小,所以0.01mol/L FeCl3溶液中Fe3+浓度小于0.1mo/L FeCl3溶液中Fe3+浓度的![]() ,故0.1mol/L的FeCl3溶液与0.01mol/L的FeCl3溶液中, Fe3+的浓度之比大于10,选项A正确;
,故0.1mol/L的FeCl3溶液与0.01mol/L的FeCl3溶液中, Fe3+的浓度之比大于10,选项A正确;
B、在25℃下,平衡时溶液中c(NH4+)=c(Cl-)=0.005mol/L,根据物料守恒得c(NH3.H2O)=(0.5a-0.005)mol/L,根据电荷守恒得c(H+)=c(OH-)=10-7mol/L,溶液呈中性,NH3H2O的电离常数Kb=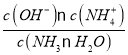 =
=![]() =
=![]() ,选项B正确;
,选项B正确;
C、pH加和为12的强酸与弱酸,因为酸的pH都小于7,则二者的pH在5-7之间,混合后pH可能为6,选项C正确;
D、0.1mol·L-1 NH4HS溶液中依据物料守恒有:c(NH3·H2O)+c(NH4+)=c(HS-)+c(S2-)+c(H2S),选项D不正确;
答案选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法不正确的是
A. 6.02×1023就是阿伏加德罗常数
B. 1 mol水中的氢原子数目为2NA
C. 阿伏加德罗常数个粒子的物质的量是1 mol
D. 1 mol 氨气所含原子数约为2.408×1024个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机制药工业中常用以下方法合成一种药物中间体(G):
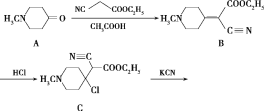
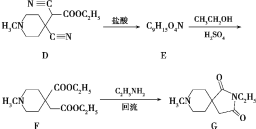
(1)G的分子式是___。
(2)化合物A中含氧官能团的名称为___。
(3)由C→D的反应类型为___;化合物E的结构简式为___。
(4)写出B→C的反应的化学方程式:___。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
①能与新制Cu(OH)2在加热条件下反应生成砖红色沉淀,水解产物之一能与FeCl3溶液发生显色反应;
②核磁共振氢谱为四组峰,峰面积比为1∶2∶4∶9;
③分子中含有氨基。
(6)已知:RCN![]() RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备
RCH2NH2,请写出以HOOCCH2CH2COOH和CH3CH2Cl为原料制备![]() 的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图___(无机试剂任用)。合成路线流程图示例如下:
CH3CH2OH![]() CH2
CH2![]() CH2
CH2![]() CH3CH2Cl
CH3CH2Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填表
微粒 | 核外电子数 | 中子数 | 质量数 | 最外层电子数 |
| __________ | ____________ | _________ | _________ |
| _________ | ___________ | _________ | ____________ |
| ___________ | ________ | ______ | ________ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为![]() ,还有少量
,还有少量![]() 、
、![]() 等杂质)为原料制备绿矾晶体
等杂质)为原料制备绿矾晶体![]() 的工艺流程如下:
的工艺流程如下:
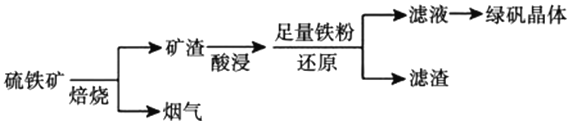
(1)“酸浸”过程,矿渣中的![]() 与稀
与稀![]() 反应的离子方程式____________________。
反应的离子方程式____________________。
(2)烟气中的![]() 会污染环境,可用足量氨水吸收。写出该反应的离子方程式____________________________。
会污染环境,可用足量氨水吸收。写出该反应的离子方程式____________________________。
(3)写出检验滤液中阴离子的方法___________________________。
(4)铁粉还原过滤,滤渣主要成分是___________________________(写化学式)。
(5)燃料细菌脱硫法是用氧化亚铁硫杄菌(T.f)对硫铁矿进行催化脱硫,同时得到![]() 溶液。其过程如图所示:
溶液。其过程如图所示:
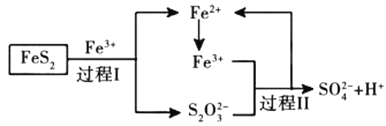
已知总反应为:![]()
写出过程Ⅱ反应的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于氧化还原反应,下列说法正确的是( )
①Mg在化学反应中失去2个电子,而Al在化学反应中失去3个电子 ,因此还原性Al>Mg;
②氧化剂具有氧化性;
③有单质参加的反应一定是氧化还原反应;
④2Fe+3Cl2![]() 2FeCl3;Fe+S
2FeCl3;Fe+S![]() FeS,由此可以判断氧化性:Cl2>S
FeS,由此可以判断氧化性:Cl2>S
⑤氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原
A.②③④ B.②④ C.①②⑤ D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示。下列说法不正确的是
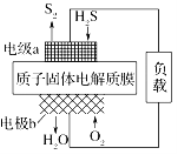
A. 电极a为电池的负极
B. 电极b上发生的电极反应为O2+4H++4e-===2H2O
C. 电路中每流过4 mol电子,在正极消耗44.8 L H2S
D. 每0.5molH2S参与反应,有1 mol H+经质子膜进入正极区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是大气污染物之一,实验室拟将
是大气污染物之一,实验室拟将![]() 与
与![]() 混合用
混合用![]() 溶液吸收的方法消除其污染。回答下列问题:
溶液吸收的方法消除其污染。回答下列问题:
(1)氯气的制备
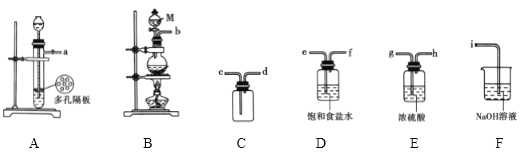
①仪器M的名称是_______________
②欲用![]() 和浓盐酸制备并收集一瓶纯净干燥的氯气,选择上图中的装置,其连接顺序为____________(按气流方向,用小写字母表示)。
和浓盐酸制备并收集一瓶纯净干燥的氯气,选择上图中的装置,其连接顺序为____________(按气流方向,用小写字母表示)。
③D在制备装置中的作用是______________;装置F的作用是__________________。
(2)用如下图所示装置,探究![]() 和
和![]() 在
在![]() 溶液中的反应。查阅有关资料可知:
溶液中的反应。查阅有关资料可知:![]() 是一种弱酸,且不稳定,易分解生成
是一种弱酸,且不稳定,易分解生成![]() 和
和![]() 。
。
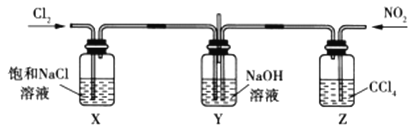
①装置中X和Z的作用是_______________
②实验时观察到X试剂瓶中有黄绿色气体,Z试剂瓶中有红棕色气体,若通入适当比例的![]() 和
和![]() ,Y中观察不到气体颜色,反应结束后加入稀硫酸无现象,则Y中发生反应的化学方程式是___________。
,Y中观察不到气体颜色,反应结束后加入稀硫酸无现象,则Y中发生反应的化学方程式是___________。
③反应结束后,取Y中溶液适量置于试管中,加入稀硫酸,若有红棕色气体产生,解释产生该现象的原因_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1molL-1NaOH溶液分别滴定20.00mL0.1molL-1的盐酸和苯甲酸溶液,滴定曲线如下图所示,下列说法正确的是

A.图Ⅰ、图Ⅱ分别是NaOH溶液滴定苯甲酸、盐酸的曲线
B.V(NaOH)=10.00mL时,滴定苯甲酸的混合溶液中c(C6H5COO-)> c(Na+)> c(H+)>c(OH-)
C.滴定苯甲酸溶液时最好选用甲基橙作指示剂
D.达到B、D状态时,NaOH溶液分别与盐酸、苯甲酸恰好发生中和反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com