
【题目】一定条件下,在体积为10L的固定容器中发生的反应:N2+3H2![]() 2NH3,反应过程如下图所示,下列说法正确的是
2NH3,反应过程如下图所示,下列说法正确的是
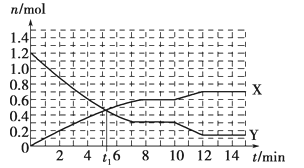
A. t1 min时正、逆反应速率相等
B. X曲线表示NH3的物质的量随时间变化的关系
C. 0~8 min,H2的平均反应速率v(H2)=0.75 mol·L-1·min-1
D. 10~12 min,N2的平均反应速率为v(N2)=0.25mol·L-1·min-1
【答案】B
【解析】试题分析: A、根据该图像,可知平衡时X的物质的量增加0.6mol,Y的物质的量减少1.2-0.3=0.9mol,0.6:0.9=2:3,说明X是氨气,Y是氢气。t1 min时X与Y的物质的量相等,但未达平衡,所以正逆反应的速率不相等,A项错误;B、X曲线表示NH3的物质的量随时间变化的关系,B项正确;C、根据A的分析可知X是氨气,正确;C、0~8 min,H2的平均反应速率v(H2)=(1.2-0.3)mol/10L/8min="0.0125" mol·L-1·min-1,C项错误;D、10~12 min,H2的平均反应速率为v(H2)=(0.3-0.15)/10L/2min="0.0075" mol·L-1·min-1,氮气的反应速率是氢气反应速率的1/3,则N2的平均反应速率为v(N2)=" 0.0075" mol·L-1·min-1/3="0.0025" mol·L-1·min-1,D项错误;答案选B。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 稀H2SO4 滴在铁片上:2Fe+6H+![]() 2Fe3++3H2↑
2Fe3++3H2↑
B. 稀盐酸滴在碳酸钙上:CO32―+2H+![]() CO2↑+H2O
CO2↑+H2O
C. 硫酸与氢氧化钡溶液混合:Ba2++SO42-![]() BaSO4↓
BaSO4↓
D. 氧化铜与盐酸反应:CuO +2H+![]() Cu2++H2O
Cu2++H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】200mL 1molL—1的氯化铝溶液中加入一定体积的2molL—1的NaOH溶液,最终产生7.8g沉淀,则加入的NaOH溶液的体积可能为
①350mL ②90mL ③150mL ④200mL
A. 只有① B. ①③ C. ②④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定质量的AlCl3和MgCl2混合溶液中逐渐滴入一定溶质质量分数的NaOH溶液,生成沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则:
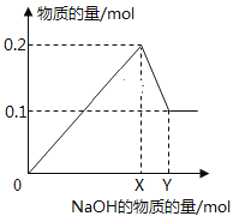
(1)O-X段反应的离子方程式为:________________________,
(2)X-Y段反应的离子方程式为_________________________
(3)生成Mg(OH)2的质量为___________________g;
(4)X=________________;Y=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示电解质溶液的导电性装置中,若向某一电解质溶液中逐滴加入另一种溶液时,则灯光由亮变暗至熄灭后又逐渐变亮的是

A. 盐酸中逐滴加入食盐溶液
B. NH4Cl溶液中加入适量的NaOH溶液
C. Ba(OH)2溶液中滴入H2SO4溶液至过量
D. 醋酸中逐滴加入氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:
①2Fe3++ H2O2 ![]() 2Fe2++O2↑+2H+
2Fe2++O2↑+2H+
② H2O2 + 2Fe2++2H+ ![]() 2H2O+2Fe3+
2H2O+2Fe3+
反应过程中能量变化如右图所示。下列说法不正确的是

A. 0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1
B. Fe3+的作用是加快过氧化氢的分解速率
C. 反应①是吸热反应、反应②是放热反应
D. 反应2H2O2(aq)![]() 2H2O(l) + O2(g)的△H =E1-E2 < 0
2H2O(l) + O2(g)的△H =E1-E2 < 0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:

①该反应为________反应(填“吸热”或“放热”)。
②若要使该反应的反应速率加快,下列措施可行的是________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(2)美国阿波罗宇宙飞船上使用了一种新型燃料电池,其构造如图所示,A、B两个电极均由多孔的碳块组成,该电池的正极反应式为:_______________________________。

(3)300 ℃时,将A和B两种气体混合于恒容密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),2 min末达到平衡。
2C(g)+2D(g),2 min末达到平衡。
①300℃时,该反应的平衡常数表达式为K=________。
②已知K300℃<K350℃,则ΔH____0(填“>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。已知多晶硅第三代工业制取流程如图所示:
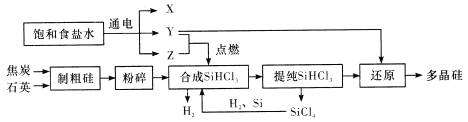
下列说法错误的是
A. Y、Z分别为H2、Cl2
B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量之比为1:1
C. SiHCl3极易水解,其完全水解的产物为H2SiO3、H2、HCl,据此推测SiHCl3中硅元素的化合价为+2价
D. Y与SiHCl3制备多晶硅的反应属于置换反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com