
【题目】短周期元素W、X、Y、Z的原子序数依次增大。W的气态氢化物遇湿润的红色石蕊试纸变蓝色,X是地壳中含量最高的元素,Y在同周期主族元素中原子半径最大,Z与Y形成的化合物的化学式为YZ。下列说法不正确的是
A.W在元素周期表中的位置是第二周期VA族
B.用电子式表示的形成过程为:![]()
C.同主族中Z的气态氢化物稳定性最强
D.X与Y形成的两种常见的化合物中,阳离子和阴离子的个数比均为2:1
【答案】C
【解析】
已知W的气态氢化物遇湿润的红色石蕊试纸变蓝色,其溶液显碱性,则该氢化物是氨气
,W是氮元素。地壳中含量最多的元素是氧,故X是氧元素。同一周期从左到右,元素的原子半径依次减小,Y在同周期主族元素中原子半径最大,则Y是第三周期的钠元素,Z也位于第三周期,Z与Y形成的化合物的化学式为YZ,钠元素的化合价为+1价,则Z元素的化合价是-1价,Z原子最外层电子数为7,它是氯元素。
A.氮是7号元素,氮原子核外电子层数为2,最外层电子数为5,它在周期表中位于第二周期VA族,故A正确;
B.钠是活泼的金属元素,氯是活泼的非金属元素,钠原子与氯原子结合时,钠原子失去电子变为钠离子,氯原子得到电子变为氯离子,两种离子之间通过离子键结合在一起,![]() ,故B正确;
,故B正确;
C.氯元素位于ⅦA族,该族元素中非金属性最强的是氟元素,非金属性越强,气态氢化物越稳定,所以最稳定,故C错误;
D.钠与氧两种元素可形成氧化物和过氧化物两种化合物,前者由钠离子与阳离子构成,后者由钠离子与过氧根离子构成,两种物质中阳离子与阴离子数之比都是,故D正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】碳、氮及其化合物在化工生产和国防工业中具有广泛应用。请回答:
(1)利用CO2的弱氧化性,开发了丙烷氧化脱氢制丙烯的新工艺。该工艺可采用铬的氧化物为催化剂,其反应机理如图:
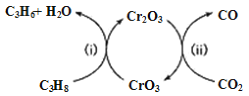
①图中催化剂为__________________。
②该工艺可以有效消除催化剂表面的积炭,维持催化剂活性,原因是______________。
(2)现向三个体积均为2L的恒容密闭容器I、Ⅱ、Ⅲ中,均分别充入1molCO和2molH2发生反应:CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为T1、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
CH3OH(g) △H1=-90.1kJ/mol。三个容器的反应温度分别为T1、T2、T3且恒定不变。当反应均进行到5min时H2的体积分数如图所示,其中只有一个容器中的反应已经达到平衡状态。
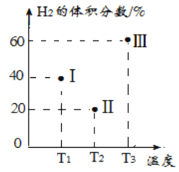
①5min 时三个容器中的反应达到化学平衡状态的是容器__________(填序号)。
②0-5min内容器I中用CH3OH表示的化学反应速率v(CH3OH)=_________。(保留两位有效数字)。
③当三个容器中的反应均达到平衡状态时,平衡常数最小的是容器_________。(填序号)
(3)在密闭容器中充入10molCO和8 molNO,发生反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g)△H=-762kJ·mo-1,如图为平衡时NO的体积分数与温度、压强的关系。
N2(g)+2CO2(g)△H=-762kJ·mo-1,如图为平衡时NO的体积分数与温度、压强的关系。
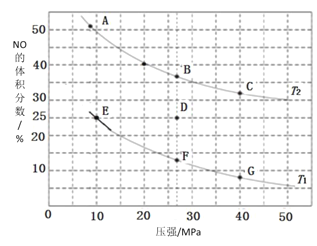
①由上图判断,温度T1_____T2(填“低于”或“高于”)。
②压强为20MPa、温度为T2下,若反应进行到10 min达到平衡状态,在该温度下,如图所示A、B、C对应的pA(CO2)、pB(CO2)、pC(CO2)从大到小的顺序为_________。
③若在D点对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的__________点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙烯(![]() )是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
)是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
![]() (g)
(g)![]()
![]() (g)+H2(g) △H
(g)+H2(g) △H
(1)已知:
化学键 | C-H | C-C | C=C | H-H |
键能/kJ/mol | 412 | 348 | 612 | 436 |
计算上述反应的△H=________ kJ·mol-1。
(2)500℃时,在恒容密闭容器中,充入a mol乙苯,反应达到平衡后容器内气体的压强为P;若再充入bmol的乙苯,重新达到平衡后容器内气体的压强为2P,则a_______b(填“>” “<”或“=”),乙苯的转化率将________(填“增大” “减小”或“不变”)。
(3)工业上,通常在乙苯(EB)蒸气中掺混N2(原料气中乙苯和N2的物质的量之比为1︰10,N2不参与反应),控制反应温度600℃,并保持体系总压为0.1Mpa不变的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图如下:
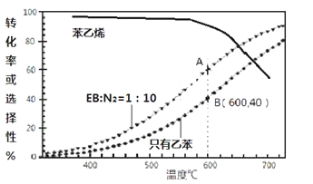
①A,B两点对应的正反应速率较大的是________。
②掺入N2能提高乙苯的平衡转化率,解释说明该事实___________________________。
③用平衡分压代替平衡浓度计算600℃时的平衡常数Kp=________。(保留两位有效数字,分压=总压×物质的量分数)
④控制反应温度为600℃的理由是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.酸性碘化钾溶液中滴加适量双氧水:2I-+2H++H2O2=I2+2H2O
B.用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
C.向苯酚钠溶液中通入少量CO2,溶液变浑浊:2![]() +CO2+H2O=2
+CO2+H2O=2![]() +CO32-
+CO32-
D.铅蓄电池充电时阴极反应式:PbSO42e-+2H2O=PbO2+SO42-+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中。下列分析正确的是( )

A. K1闭合,铁棒上发生的反应为2H++2e-=H2↑
B. K1闭合,石墨棒周围溶液pH逐渐降低
C. K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法
D. K2闭合,电路中通过0.4NA个电子时,两极共产生4.48L气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是

A.该反应的化学方程式为6A+2D![]() 3B+4C
3B+4C
B.0~1s内,v(A)=v(B)
C.5s时,v(A)=v(B)=v(C)=v(D)
D.0~5s内,B的平均反应速率为0.06mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《自然》杂志曾报道我国科学家通过测量SiO2中26Al和10Be两种元素的比例确定“北京人”年龄的研究结果,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)l0Be和9Be___(填序号)。
a.是同一种原子 b.具有相同的中子数
c.具有相同的化学性质 d.互为同位素
(2)写出A1(OH)3与NaOH溶液反应的化学方程式:___。
(3)研究表明28A1可以衰变为26Mg,可以比较这两种元素金属性强弱的方法是__(填序号)。
a.比较Mg(OH)2与A1(OH)3的碱性强弱
b.比较这两种元素的最高正化合价
c.将打磨过表面积相同的镁条和铝片分别和100℃热水作用,并滴入酚酞溶液
d.比较这两种金属的硬度和熔点
(4)目前还有一种测量方法叫“钾氩测年法”。
两种常见简单阴离子的核外电子排布与Ar相同,两者的半径大小关系为:___(用化学符号表示);其中一种离子与钾同周期相邻元素的离子所形成的化合物可用作干燥剂,用电子式表示该物质的形成过程:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是三种原子序数依次递增的前10号元素,X的某种同位素不含中子,Y形成的单质在空气中体积分数最大,三种元素原子的最外层电子数之和为12,其对应的单质及化合物转化关系如图所示。下列说法不正确的是

A.原子半径:X<Z<Y,简单气态氢化物稳定性:Y<Z
B.A、C均为10电子分子,A的沸点低于C的沸点
C.同温同压时,B与D体积比≤1∶1的尾气,可以用NaOH溶液完全处理
D.E和F均属于离子化合物,二者组成中阴、阳离子数目之比均为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究反应![]() (aq)+2I(aq)
(aq)+2I(aq)![]() 2
2![]() (aq)+I2(aq)的反应机理及反应进程中的能量变化,在
(aq)+I2(aq)的反应机理及反应进程中的能量变化,在![]() 和I的混合溶液中加入Fe3+,过程及图像如下:
和I的混合溶液中加入Fe3+,过程及图像如下:
步骤①:2Fe3+(aq)+2I(aq)![]() I2(aq)+2Fe2+(aq)
I2(aq)+2Fe2+(aq)
步骤②:2Fe2+(aq)+![]() (aq)
(aq)![]() 2Fe3+(aq)+2
2Fe3+(aq)+2![]() (aq)
(aq)
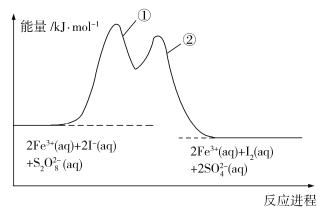
下列有关该反应的说法正确的是______
A.步骤①和②都是吸热反应
B.Fe3+是该反应的中间产物
C.步骤①比②所需活化能大
D.该反应可设计成原电池
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com