
| A. | 钠和镁分别与冷水反应,判断钠和镁金属性强弱 | |
| B. | 在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属性强弱 | |
| C. | 硅酸钠溶液中通入CO2产生白色沉淀,判断碳酸与硅酸的酸性强弱 | |
| D. | Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱 |
分析 A、金属与水反应置换出氢气的难易程度,能判断金属性的强弱;
B、元素的金属性越强,其最高价氧化物的水化物碱性越强;
C、非金属最高价氧化物对应的水化物的酸性越强,元素的非金属性越强;
D、单质与氢气化合越容易,非金属性越强.
解答 解:A、钠与冷水比镁与冷水反应剧烈,因此钠的金属性强于镁,故A正确;
B、元素的金属性越强,其最高价氧化物的水化物碱性越强,氨气和氯化镁、氯化铝溶液都反应生成氢氧化镁、氢氧化铝沉淀,不能确定氢氧化铝、氢氧化镁碱性强弱,则不能确定两种金属的金属性强弱,故B错误;
C、CO2通入硅酸钠溶液,发生强酸制取弱酸的反应,生成硅酸沉淀,可知碳酸的酸性大于硅酸,则非金属性C大于Si,故C正确;
D、卤素单质与氢气化合越容易,非金属性越强,所以能根据Br2与I2分别与足量的H2反应,判断溴与碘的非金属性强弱,故D正确.
故选B.
点评 本题考查了金属性和非金属性强弱的比较方法,题目难度不大,侧重于基础知识的考查,注意有关规律的归纳整理.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 分散质直径介于1 nm-100 nm之间的分散系称为胶体 | |
| B. | Fe(OH)3难溶于水,因此不可能均匀分散在水里形成稳定的红褐色的液体 | |
| C. | 氢氧化铁胶体粒子在电泳实验中向阴极移动,是因为氢氧化铁胶体粒子带负电 | |
| D. | 胶体粒子是很多分子的集合体,因此都很不稳定,容易聚沉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4=2Na++SO4-2 | B. | Ba(OH)2=Ba2++OH2- | ||
| C. | Fe2(SO4)3=2Fe3++3SO42- | D. | Ca(NO3)2=Ca2++2(NO3)- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 编号 | 实验温度 /℃ | Na2S2O3 | H2SO4 | 蒸馏水体积 /mL | ||
| 体积/mL | 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | |||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| ③ | 25 | 5 | 0.2 | 10 | 0.2 | 5 |
| ④ | 50 | 5 | 0.1 | 10 | 0.1 | 5 |
| ⑤ | 50 | 10 | 0.2 | 5 | 0.2 | 5 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
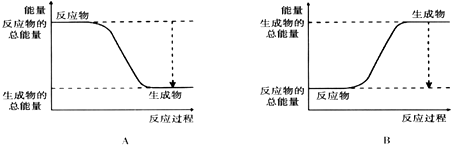
| 化学键 | H-H | O=O | H-O |
| 键能kJ.mol-1 | 436 | 496 | 463 |
| 化学键 | 填“吸收热量” 或“放出热量” | 能量变化kJ | |
拆开化学键 | 2molH2和1molO2中的化学键 | ||
| 形成化学键 | 4molH-O键 | ||
| 总能量变化 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯不能使酸性KMnO4溶液褪色,与甲烷性质相似,因此苯为饱和烃 | |
| B. | 苯的结构简式为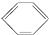 有三个双键,可与溴水发生加成反应 有三个双键,可与溴水发生加成反应 | |
| C. | 苯的6个碳原子和6个氢原子在同一平面内 | |
| D. | 将1 mL苯和1 mL水充分混合后静置,二者互溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
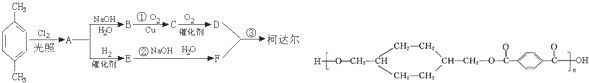
 ;D
;D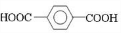 ;E
;E
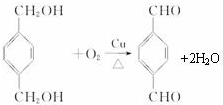 ,反应类型氧化反应
,反应类型氧化反应 ,反应类型取代反应
,反应类型取代反应 +
+ $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$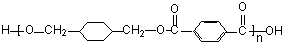 +(2n-1)H2O,反应类型缩聚反应.
+(2n-1)H2O,反应类型缩聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
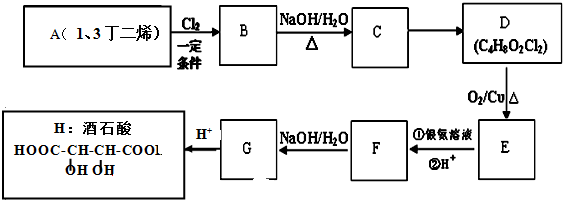

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com